(Cánh diều) Lý thuyết KHTN 8 Bài 4: Mol và tỉ khối của chất khí
Tóm tắt Lý thuyết Khoa học tự nhiên 8 Cánh Diều Bài 4. Mol và tỉ khối của chất khí theo chương trình Sách mới ngắn gọn nhất. Tổng hợp lý thuyết Khoa học tự nhiên 8 trọn bộ chi tiết, đầy đủ.
Bài 4. Mol và tỉ khối của chất khí
Soạn Khoa học tự nhiên 8 Cánh Diều Bài 4
I. Khái niệm mol
- Mol là lượng chất có chứa 6,022 × 10^23 hạt vi mô (nguyên tử, phân tử,...) của chất đã được định nghĩa bằng hằng số Avogado.
II. Khối lượng mol
- Khối lượng mol (M) của một chất là khối lượng tỉnh bằng gam của N nguyên tử hoặc phân tử chất đến NAvogado, có đơn vị là gam/mol.
III. Chuyển đổi giữa số mol chất và khối lượng
- Ví dụ: Đốt cháy hoàn toàn 6 gam carbon với oxygen. Tính số mol. Biết khối lượng mol của carbon là 12 gam/mol.
Số mol carbon cần tìm là n. Ta có: 1 mol carbon nặng 12 gam, a mol carbon nặng 6 gam.
Vậy n = 0,5 (mol).
- Tổng quát, nếu đặt n là số mol chất, M là khối lượng một chất và m là khối lượng chất, ta có công thức:
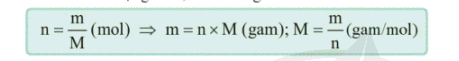
IV. Thể tích mol của chất khí
- Một mol của bất kì chất khí nào ở cùng điều kiện nhiệt độ và áp suất sẽ chiếm một thể tích nhất định, ví dụ: 1 mol He chiếm 24,79 L, 1 mol O2 chiếm 24,79 L.
V. Chuyển đổi giữa lượng chất và thể tích chất khí
- Ở điều kiện chuẩn (đkc), mối liên hệ giữa số mol và thể tích của các chất khí được biểu diễn trong bảng 4.1. Đặt n là số mol chất khí, V là thể tích chất khí ở đkc, ta có biểu thức: n = V/Vm, với Vm là thể tích một mol chất khí ở đkc.

VI. Tỉ khối của chất khí
- Tỉ khối của khi A so với khi B là tỉ số giữa khối lượng mol của khi A và khối lượng mol của khí B.
- Tỉ khối của khi A so với khí B được kí hiệu là dA/B và được tính bằng biểu thức

- Tỉ khối của khi A so với khi B cho biết khi A nặng hay nhẹ hơn khi B bao nhiêu lần.
- Để biết khi X nặng hay nhẹ hơn không khí bao nhiêu lần, ta so sánh khối lượng mol của khí X (Mx) với khối lượng mol trung bình của không khí là 29 g/mol: dx = Mx/29.
VII. Trắc nghiệm Khoa học tự nhiên 8 Cánh diều Bài 4 (có đáp án)
Câu 1: Khối lượng mol kí hiệu là gì?
A. N
B. M
C. Ml
D. Mol
Câu 2: Ở điều kiện chuẩn, 1 mol khí bất kì chiếm thể tích bao nhiêu?
A. 24,97l
B. 27,94l
C. 24,79l
D. 27,49l
Giải thích:
1 mol khí bất kì chiếm thể tích là 24,79l với điều kiện phải ở nhiệt độ 0oC và áp suất là 1 atm gọi là điều kiện chuẩn của môi trường (đktc)
Câu 3: Hợp chất khí X có tỉ khối so với hiđro bằng 22. Công thức hóa học của X có thể là
A. NO2
B. CO2
C. NH3
D. NO
Giải thích:
Hợp chất khí X có tỉ khối so với hidro bằng 22, ta có:
dX/H2 = MX/MH2 => 22 = MX/2 => MX = 44
Vậy công thức hóa học của X có thể là CO2
Câu 4: Khối lượng mol chất là
A. Là khối lượng ban đầu của chất đó
B. Là khối lượng sau khi tham gia phản ứng hóa học
C. Bằng 6.1023
D. Là khối lượng tính bằng gam của N nguyên tử hoặc phân tử chất đó
Câu 5: Tỉ khối hơi của khí lưu huỳnh (IV) oxit (SO2) đối với khí clo (Cl2) là:
A. 0,19
B. 1,5
C. 0,9
D. 1,7
Giải thích:
Ta có: MSO2 = 64 và MCl2 = 71.
Áp dụng công thức tỷ khối hơi: dMSO2/ MCl2 = 64/71 = 0,9
Vậy tỉ khối hơi của khí lưu huỳnh (IV) oxit (SO2) đối với khí clo (Cl2) là: 0,9.
>>> Xem toàn bộ: Lý thuyết Khoa học tự nhiên 8 Cánh Diều
-------------------------------------------
Trên đây Toploigiai đã cùng các bạn Lý thuyết Khoa học tự nhiên 8 Cánh Diều Bài 4. Mol và tỉ khối của chất khí theo chương trình Sách mới ngắn gọn nhất. Mời các bạn hãy click ngay vào trang chủ Toploigiai để tham khảo và chuẩn bị bài cho năm học mới Lớp 8 nhé. Chúc các bạn học tốt.
