(Cánh diều) Lý thuyết KHTN 8 Bài 5: Tính theo phương trình hóa học
Tóm tắt Lý thuyết Khoa học tự nhiên 8 Cánh Diều Bài 5. Tính theo phương trình hóa học theo chương trình Sách mới ngắn gọn nhất. Tổng hợp lý thuyết Khoa học tự nhiên 8 trọn bộ chi tiết, đầy đủ.
Bài 5. Tính theo phương trình hóa học
Soạn Khoa học tự nhiên 8 Cánh diều Bài 5: Tính theo phương trình hóa học
I. Xác định khối lượng, số Mol của chất phản ứng và sản phẩm trong phản ứng hóa học
Các bước tính số mol:
- Viết phương trình hoá học của phản ứng
- Tính số mol chất đã biết dựa vào khối lượng hoặc thể tích
- Dựa vào phương trình hoá học và số mol chất đã biết để tìm số mol chất tham gia phản ứng hoặc chất sản phẩm
- Tính khối lượng hoặc thể tích của chất cần tìm
II. Hiệu suất phản ứng
Xét phản ứng
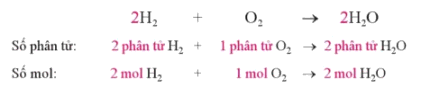
- Chất phản ứng hết là chất không còn sau khi phản ứng kết thúc.
- Chất phản ứng dư là chất còn lại sau khi kết thúc phản ứng.
- Lượng chất sản phẩm tạo thành được tính theo chất phản ứng hết.
- Hiệu suất phản ứng là tỉ số giữa lượng sản phẩm thu được theo thực tế và lượng sản phẩm thu được theo lí thuyết.
- Hiệu suất phản ứng biểu thị theo phần trăm và được tính theo công thức:
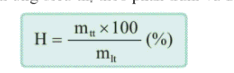
trong đó mtt là khối lượng chất (g) thu được theo thực tế và mlt, là khối lượng chất (g) thu được theo lí thuyết (tính theo phương trình).
III. Trắc nghiệm Khoa học tự nhiên 8 Cánh diều Bài 5 (có đáp án)
Câu 1: Khi đốt than (thành phần chính là cacbon), phương trình hóa học xảy ra như sau: C + O2 → CO2. Nếu đem đốt 3,6 gam cacbon thì lượng khí CO2 sinh ra sau phản ứng ở điều kiện tiêu chuẩn là là?
A. 3,36 lít
B. 4,48 lít
C. 6,72 lít
D. 5,6 lít
Giải thích:
Số mol của C là:
nC = 3,6/12 = 0,3 mol
Phương trình phản ứng:
C + O2 → CO2
0,3 0,3mol
Theo phương trình phản ứng ta có
nCO2= 0,3 mol
Vậy thể tích khí CO2 ở đktc là:
V = 0,3.22,4 = 6,72 lít.
Câu 2: Cho 98g H2SO4 loãng 20% phản ứng với thanh nhôm thấy có khí bay lên. Xác định thể tích khí đó
A. 4,8 lít
B. 2,24 lít
C. 4,48 lít
D. 0,345 lít
Giải thích:
Ta có số mol của H2SO4 là: nH2SO4 = (20%.98)/98.100 = 0,2 mol
PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
0,2 → 0,2 (mol)
Vậy thể tích của H2 là: VH2 = 0,2.22,4 = 4,48 lít
Câu 3: Đơn vị của khối lượng mol chất là:
A. gam
B. gam/mol
C. mol/gam
D. kilogam
Câu 4: Cho 5,6 g sắt tác dụng với dung dịch axit clohidric loãng thu được bao nhiêu ml khí H2
A. 2,24 ml
B. 22,4 ml
C. 2, 24.10−3 ml
D. 0,0224 ml
Giải thích:
Theo bài ra, ta có:
mFe = 5,6 => nFe = mFe/MFe = 5,6/56 = 0,1 mol
PTHH: Fe + 2HCl → FeCl2 + H2
0,1 0,1 (mol)
=> VH2 = nH2. 22,4 = 0,1.22,4 = 2,24 l
Câu 5: Khẳng định nào dưới đây không đúng khi nói về tính toán theo phương trình hóa học?
A. Tính toán theo phương trình cần viết phương trình hóa học của phản ứng xảy ra.
B. Tính toán theo phương trình cần viết sơ đồ phản ứng xảy ra.
C. Sử dụng linh hoạt công thức tính khối lượng hoặc tính thể tích ở điều kiện tiêu chuẩn.
D. Cần tiến hành tính số mol của các chất tham gia hoặc sản phẩm trước khi tính toán theo yêu cầu của đề bài.
>>> Xem toàn bộ: Lý thuyết Khoa học tự nhiên 8 Cánh Diều
-------------------------------------------
Trên đây Toploigiai đã cùng các bạn Lý thuyết Khoa học tự nhiên 8 Cánh Diều Bài 5. Tính theo phương trình hóa học theo chương trình Sách mới ngắn gọn nhất. Mời các bạn hãy click ngay vào trang chủ Toploigiai để tham khảo và chuẩn bị bài cho năm học mới Lớp 8 nhé. Chúc các bạn học tốt.
