Soạn KHTN 8 Cánh diều Bài 4: Mol và tỉ khối của chất khí
Hướng dẫn Soạn KHTN 8 Cánh diều Bài 4: Mol và tỉ khối của chất khí ngắn gọn, hay nhất theo chương trình Sách mới.
Bài 4: Mol và tỉ khối của chất khí
Lý thuyết Khoa học tự nhiên 8 Cánh Diều Bài 4: Mol và tỉ khối của chất khí
Mở đầu trang 27 Bài 4 KHTN lớp 8: Nếu yêu cầu đếm số lượng viên gạch để xây bức tường của lâu đài (hình 4.1) và đếm số lượng hạt cát để xây bức tường của lâu đài bằng cát (hình 4.2), yêu cầu nào có thể thực hiện được? Vì sao?
Với những vật thể có kích thước và khối lượng đáng kể như viên gạch, quả táo, …, người ta dễ dàng xác định số lượng, khối lượng và thể tích của chúng bằng cách đếm, cân, đo, … Nhưng với những hạt có kích thước vô cùng nhỏ bé như nguyên tử, phân tử rất khó có thể cân và đếm được chúng.
Vậy làm thế nào để có thể xác định một cách thuận lợi số nguyên tử, phân tử và khối lượng, thể tích của chúng khi tham gia và tạo thành trong các phản ứng hoá học?

Trả lời:
- Yêu cầu đếm số lượng viên gạch có thể thực hiện được do viên gạch có kích thước cụ thể và đáng kể, có thể dễ dàng xác định được số lượng.
- Để xác định một cách thuận lợi số nguyên tử, phân tử và khối lượng, thể tích của chúng khi tham gia và tạo thành trong các phản ứng hoá học ta dùng khái niệm mol.
Câu hỏi 1 trang 27 KHTN lớp 8: Xác định số nguyên tử có trong:
a) 2 mol nguyên tử nhôm (aluminium).
b) 1,5 mol nguyên tử carbon.
Trả lời:
Áp dụng: Mol là lượng chất có chứa 6,022 × 1023 hạt vi mô (nguyên tử, phân tử, …) của chất đó.
a) Số nguyên tử có trong 2 mol nguyên tử nhôm (aluminium):
2 × 6,022 × 1023 = 1,2044 × 1024 (nguyên tử).
b) Số nguyên tử có trong 1,5 mol nguyên tử carbon:
1,5 × 6,022 × 1023 = 9,033 × 1023 (nguyên tử).
Luyện tập 1 trang 28 KHTN lớp 8: Tính số phân tử nước và số nguyên tử của mỗi nguyên tố có trong 3 mol phân tử nước.
Trả lời:
- 3 mol phân tử nước chứa số phân tử nước là:
3 × 6,022 × 1023 = 1,8066 × 1024 (phân tử).
- Cứ 1 phân tử nước chứa 2 nguyên tử hydrogen và 1 nguyên tử oxygen.
Vậy 3 mol phân tử nước chứa:
+ Số nguyên tử hydrogen là: 2 × 1,8066 × 1024 = 3,6132 × 1024 (nguyên tử).
+ Số nguyên tử oxygen là: 1 × 1,8066 × 1024 = 1,8066 × 1024 (nguyên tử).
Câu hỏi 2 trang 28 KHTN lớp 8: Quan sát hình 4.3, cho biết khối lượng 1 mol nguyên tử đồng và khối lượng 1 mol phân tử sodium chloride.

Trả lời:
Khối lượng 1 mol nguyên tử đồng là 64 gam
Khối lượng 1 mol phân tử Sodium chloride là 58,5 gam
Câu hỏi 3 trang 28 KHTN lớp 8: Dựa vào bảng tuần hoàn các nguyên tố hoá học, cho biết khối lượng mol nguyên tử hydrogen, nitơ (nitrogen) và magnesium.
Trả lời:
Dựa vào bảng tuần hoàn:
- Khối lượng mol nguyên tử hydrogen là: 1,008 (gam/ mol).
- Khối lượng mol nguyên tử nitơ (nitrogen) là: 14,01 (gam/ mol).
- Khối lượng mol nguyên tử magnesium là: 24,31 (gam/ mol).
Luyện tập 2 trang 28 KHTN lớp 8: Tính khối lượng mol phân tử khí oxygen và khí carbon dioxide.
Trả lời:
Áp dụng: Khối lượng mol phân tử của một chất có cùng trị số với khối lượng phân tử chất đó tính theo đơn vị amu.
Vậy:
Khối lượng mol phân tử khí oxygen là: 16 × 2 = 32 (gam/ mol).
Khối lượng mol phân tử khí carbon dioxide là: 12 + 16 × 2 = 44 (gam/ mol).
Tìm hiểu thêm trang 28 KHTN lớp 8: Giải thích vì sao khối lượng mol nguyên tử hay phân tử của một chất có cùng trị số với khối lượng nguyên tử hay phân tử chất đó tính theo đơn vị amu.
Trả lời:
Ta có: 1 amu = 1,6605 × 10-24 gam.
Với một nguyên tử/ phân tử có khối lượng là M (amu), ta có khối lượng mol nguyên tử/ phân tử đó là:
M × 1,6605 × 10-24 × 6,022 × 1023 ≈ M (gam/ mol).
Vậy ta có điều cần chứng minh.
Luyện tập 3 trang 29 KHTN lớp 8: Hoàn thành những thông tin còn thiếu trong bảng sau:
Chất |
Số mol |
Khối lượng mol |
Khối lượng |
Cách tính |
| Nhôm | 0,2 | 27 | 5,4 | mAl = 0,2 . 27 = 5,4 (gam) |
| Nước | 2 | ? | ? | ? |
| Khí oxygen | ? | ? | 16 | ? |
| Khí nitơ | ? | ? | 28 | ? |
| Sodium chloride | 0,4 | ? | ? | ? |
| Magnesium | ? | ? | 12 | ? |
Trả lời:
Chất |
Số mol (n) (mol) |
Khối lượng mol (M) (g/mol) |
Khối lượng (m) (gam) |
Cách tính |
| Nhôm | 0,2 | 27 | 5,4 | mAl = 0,2 . 27 = 5,4 (gam) |
| Nước | 2 | 18 | 36 | mH2O = 2. 18 = 36 (gam) |
| Khí oxygen | 0,5 | 32 | 16 | nO2 = 16/32 = 0,5 mol |
| Khí nitơ | 1 | 28 | 28 | nN2 = 28/28 = 1 mol |
| Sodium chloride | 0,4 | 58,5 | 23,52 | mNaCl = 0,4. 58,5 = 23,52 (gam) |
| Magnesium | 0,5 | 24 | 12 | nMg = 12/24 = 0,5 mol |
Câu hỏi 4 trang 29 KHTN lớp 8: Quan sát hình 4.4, cho biết ở điều kiện chuẩn (áp suất 1 bar và nhiệt độ 25 oC), thể tích 1 mol khí là bao nhiêu?

Trả lời:
Ở điều kiện chuẩn (áp suất 1 bar và nhiệt độ 25 oC), thể tích 1 mol khí là 24,79 lít.
Luyện tập 4 trang 30 KHTN lớp 8: Hoàn thành những thông tin còn thiếu trong bảng sau:
| Chất | Các đại lượng (đơn vị) | |||
| M (g/mol) | n (mol) | m (g) | V (l) (đkc) | |
| CO2 | ? | ? | 17,6 | ? |
| N2 | ? | ? | ? | 4,958 |
| H2? | ? | 0,5 | ? | ? |
Trả lời:
| Chất | Các đại lượng (đơn vị) | |||
| M (g/mol) | n (mol) | m (g) | V (l) (đkc) | |
| CO2 | 44 | 0,4 | 17,6 | 9,916 |
| N2 | 28 | 0,2 | 5,6 | 4,958 |
| H2 | 2 | 0,5 | 1 | 12,395 |
Câu hỏi 5 trang 30 KHTN lớp 8: Nếu không dùng cân, làm thế nào có thể biết được 24,79 lít khí N2 nặng hơn 24,79 lít khí H2 bao nhiêu lần (ở cùng điều kiện nhiệt độ, áp suất)?
Trả lời:
2 khí có cùng thể tích là 24,79 lit (thể tích mol)
Nếu không dùng cân người ta có thể tính khối lượng mol của khí H2 và N2 (ở cùng điều kiện nhiệt độ, áp suất) thấy khối lượng mol của N2 nặng hơn H2 14 lần (28/2 = 14).
Câu hỏi 6 trang 30 KHTN lớp 8: Làm thế nào để biết khí A nặng hay nhẹ hơn khí B?
Trả lời:
So sánh khí A nặng hay nhẹ hơn khí B người ta dùng tỉ khối của khí A đối với khí B (là tỉ số giữa khối lượng mol của khí A với khối lượng mol của khí B)
Luyện tập 5 trang 31 KHTN lớp 8: Có ba quả bóng bay giống nhau về kích thước và khối lượng. Lần lượt bơm cùng thể tích mỗi khí H2, CO2, O2 vào từng quả bóng bay trên. Điều gì sẽ xảy ra khi thả ba quả bóng bay đó trong không khí?
Trả lời:
Khi thả ba quả bóng bay vào không khí chỉ có quả bóng bay chứa khí H2 là bay được lên, còn quả bóng chứa khí O2 và quả bóng chứa khí CO2 đều rơi xuống mặt đất. Do khí H2 nhẹ hơn không khí còn khí O2 và khí CO2 đều nặng hơn không khí.
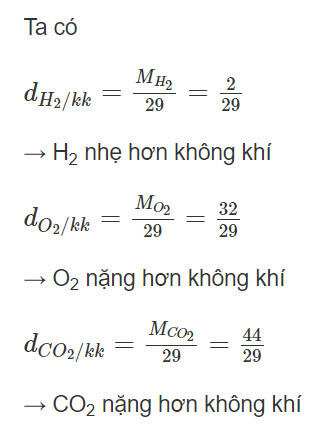
Vậy khi thả 3 quả bóng ra sẽ thấy: quả bóng chứa khí H2 bay lên còn khi CO2, O2 thì rơi xuống đất
>>> Xem toàn bộ: Soạn KHTN 8 Cánh Diều
-------------------------------------
Trên đây Toploigiai đã cùng các bạn Trả lời câu hỏi KHTN 8 Cánh Diều Bài 4: Mol và tỉ khối của chất khí trong bộ SGK Cánh Diều theo chương trình sách mới. Chúc các bạn học tốt!
