Trắc nghiệm Đúng sai Trả lời ngắn Hóa 10 Bài 12: Phản ứng oxi hóa - khử
Tổng hợp 20 câu Trắc nghiệm Đúng sai Trả lời ngắn Hóa 10 Bài 12: Phản ứng oxi hóa - khử có đáp án chi tiết bám sát chương trình học Sách mới năm học 2024-2025
Phần 1. Trắc nghiệm Đúng Sai
Câu 1. Trong phản ứng oxi hóa – khử thì
A. Số oxi hóa của nguyên tử trong bất kì đơn chất hóa học nào đều bằng 0.
B. Tổng số oxi hóa của tất cả các nguyên tử trong một phân tử và trong ion đa nguyên tử bằng 0.
C. Trong tất cả các hợp chất, hydrogen luôn có số oxi hóa là +1.
D. Trong tất các các hợp chất, oxygen luôn có số oxi hóa là -2.
A. đúng
Câu 2. Cảnh sát giao thông sử dụng các dụng cụ phân tích rượu etylic có chứa CrO3. Khi tài xế hà hơi thở vào dụng cụ phân tích trên, nếu trong hơi thở có chứa hơi rượu thì hơi rượu sẽ tác dụng với CrO3 có màu da cam và biến thành Cr2O3 có màu xanh đen theo phản ứng hóa học sau:
CrO3 + C2H5OH → CO2↑ + Cr2O3 + H2O
A. Tỉ lệ chất khử: chất oxi hóa ở phương trình hóa học trên là 1: 4.
B. Trong phản ứng trên thì CrO3 đóng vai trò là chất khử.
C. Tỉ lệ cân bằng của phản ứng trên là 4 : 1 : 2 : 2 : 3.
D. Số oxi hóa của Carbon trước và sau phản ứng lần lượt là +2 và +4.
C. đúng
D. đúng
Câu 3. “Calcium chloride dùng trong điện phân để sản xuất calcium kim loại và điều chế các hợp kim của calcium. Với tính chất hút ẩm lớn, calcium chloride được dùng làm tác nhân sấy khí và chất lỏng. Do nhiệt độ đông đặc thấp nên dung dịch calcium chloride được dùng làm chất tải lạnh trong các hệ thống lạnh…. Ngoài ra, calcium chloride còn được làm chất keo tụ trong hóa dược và dược phẩm hay trong các công việc khoan dầu khí. Trong phản ứng tạo thành Calcium chloride từ đơn chất: Ca + Cl2 → CaCl2.
A. Trong phản ứng trên thì mỗi nguyên tử Calcium nhường 2e.
B. Số oxi hóa của Ca và Cl trước phản ứng lần lượt là +2 và -1.
C. Nếu dùng 4 gam Calcium thì số mol electron Chlorine nhận là 0,4 mol.
D. Liên kết trong phân tử CaCl2 là liên kết ion.
A. đúng
D. đúng
Câu 4. Trong một phản ứng oxi hóa – khử:
A. Chất khử (chất bị oxi hóa) là chất nhường electron và chất bị oxi hóa (chất bị khử) là chất nhận electron.
B. Quá trình nhường electron là quá trình khử và quá trình nhận electron là quá trình oxi hóa.
C. Trong quá trình oxi hóa, chất oxi hóa bị oxi hóa lên số oxi hóa cao hơn.
D. Phản ứng trong đó có sự trao đổi (nhường – nhận) electron là phản ứng oxi hóa - khử.
A. đúng
D. đúng
Câu 5. Trong thiên nhiên manganesium là nguyên tố tương đối phổ biến đứng thứ ba trong các kim loại chuyển tiếp, chỉ sau Fe và Ti. Các khoáng vật chính của manganesium là hausmanite (Mn3O4), pyrolusite (MnO2), braunite (Mn2O3) và manganite (MnOOH). Manganesium tồn tại ở rất nhiều trạng thái oxi hóa khác nhau từ +2 tới +7.
A. Mn có thể đóng vai trò vừa là chất khử, vừa là chất oxi hóa.
B. Trong pyrolusite - MnO2 thì Mn có số oxi hóa là + 4.
C. Nếu thực hiện phản ứng từ MnO2 chuyển hóa thành KMnO4 thì nguyên tử Mn đã nhận 3 electron.
D. Trong manganite (MnOOH) thì Mn có thể xảy ra quá trình oxi hóa khi tham gia phản ứng.
A. đúng
B. đúng
D. đúng
Câu 6. Xăng E5 là một loại xăng sinh học, được tạo thành khi trộn 5 thể tích ethanol với 95 thể tích xăng truyền thống, giúp thay thế một phần nhiên liệu hóa thạch, phù hợp với xu thế phát triển chung trên thế giới và góp phần đảm bảo an ninh năng lượng quốc gia.Trong phương trình đốt cháy ethanol thành CO2 và H2O thì
A. Phản ứng này không phải là phản ứng oxi hóa khử.
B. Phản ứng này giải phóng năng lượng ra môi trường dưới dạng nhiêt.
C. Tổng hệ số cân bằng của phản ứng trên là 9.
D. Ethanol đóng vai trò là chất khử.
B. đúng
C. đúng
D. đúng
Câu 7. Rượu gạo là một thức uống có cồn lên men được chưng cất từ gạo theo truyền thống. Rượu gạo được làm từ quá trình lên men tinh bột gạo đã được chuyển thành đường. Vi khuẩn là nguồn gốc gốc của các enzyme chuyển đổi tinh bột thành đường. Nhiệt độ thích hợp để lên men rượu khoảng 20 – 250C. Phản ứng thủy phân và lên men:
theo truyền thống. Rượu gạo được làm từ quá trình lên men tinh bột gạo đã được chuyển thành đường. Vi khuẩn là nguồn gốc gốc của các enzyme chuyển đổi tinh bột thành đường. Nhiệt độ thích hợp để lên men rượu khoảng 20 – 250C. Phản ứng thủy phân và lên men:
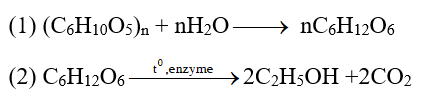
A. Phản ứng (2) là phản ứng oxi hóa – khử, do có sự thay đổi số oxi hóa của C.
B. Trong phản ứng (2) thì C6H12O6 vừa là chất khử, vừa là chất oxi hóa.
C. Trong phản ứng (1) thì các nguyên tử của mỗi nguyên tố không thay đổi số oxi hóa.
D. Trong phản ứng (2) thì nguyên tử Carbon đã nhận 4 electron.
A. đúng
B. đúng
C. đúng
Câu 8. Quá trình đốt cháy nhiên liệu (khí đốt, xăng, dầu hoặc khí hóa lỏng) là một ví dụ về sự cháy của hydrocarbon trong oxygen và cung cấp cho chúng ta năng lượng. Nếu oxygen dư thì sự cháy xảy ra hoàn toàn và cho sản phẩm là CO2 và nước. Nếu không dư oxygen, sự cháy xảy ra không hoàn toàn và một phần carbon chuyển thành CO là một khí độc, gây ô nhiễm môi trường. Còn khi rất thiếu oxygen thì chỉ tạo ra nước và để lại muội là carbon. Phản ứng cháy của xăng (octane – C8H18) trong ba điều kiện:
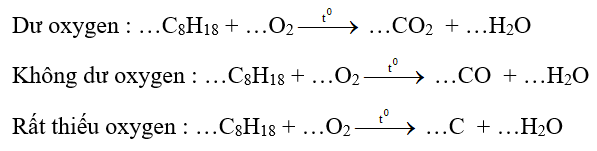
A. Trong điều kiện cháy dư oxygen, một phân tử C8H18 nhường 50 electron.
B. Trong các phản ứng thì Oxygen đóng vai trò là chất oxi hóa.
C. Trong điều kiện cháy thiếu oxygen sẽ tiết kiệm năng lượng nhất và không gây ô nhiễm môi trường.
D. Trong điều kiện cháy không dư oxygen thì tỉ lệ cân bằng là 2 : 15 : 16 : 9.
A. đúng
B. đúng
Câu 9. Nitric acid (HNO3) là hợp chất vô cơ, trong tự nhiên được hình thành trong những cơn mưa giông kèm sấm chớp. Nitric acid là một acid độc, ăn mòn và dễ gây cháy, là một trong những tác nhân gây ra mưa acid.

Thực hiện thí nghiệm xác định công thức của một oxide của kim loại sắt bằng nitric acid đặc nóng, thu được 2,479 lít (đkc) khí màu nâu là nitrogen dioxide. Phần dung dịch đem cô cạn thì được 72,6 gam Fe(NO3)3. Giả sử phản ứng không tạo thành các sản phẩm khác (biết 1 mol khí chiếm 24,79 lít đo ở đkc 250C, 1 bar).
A. Trong phản ứng trên thì FexOy là chất khử và HNO3 là chất oxi hóa.
B. FexOy(s) + (6x -2y) HNO3 (aq) → xFe(NO3)3 (aq) + (3x -2y)NO2(g) + (3x –y)H2O(l).
C. Trong phản ứng trên thì nguyên tử N trong HNO3 đã nhận 3 electron.
D. Iron oxide đã sử dụng trong phản ứng trên là Fe2O3.
A. đúng
B. đúng
Câu 10. Chromium là một trong những kim loại có độ cứng lớn nhất. Cụm từ chromium xuất phát từ tiếng Hy Lạp, có nghĩa là ”màu sắc” do các hợp chất của chromium thường có màu sắc rất đậm. Cho thấy màu sắc một số hợp chất của chromium theo thứ tự CrCl2, CrCl3, K2CrO4, K2Cr2O7.

A. Số oxi hóa của Cr trong các hợp chất CrCl2, CrCl3, K2CrO4, K2Cr2O7 lần lượt là +2, +3, +6, +6.
B. Trong phản ứng K2Cr2O7 + 14HCl → 2CrCl3 + 2KCl + 3Cl2↑ + 7H2O thì nguyên tử Chromium đã nhận 3 electron.
C. Trong dung dịch có cân bằng: 2CrO42- + 2H+ ⇆ Cr2O72- + H2O thì số oxi hóa Chromium không thay đổi.
D. Tỉ lệ cân bằng của phản ứng CrO3 + C2H5OH → CO2 ↑ + Cr2O3+ H2O là 2 : 1 : 2 : 3 : 3.
A. đúng
B. đúng
C. đúng
Phần 2. Câu hỏi Trả lời ngắn
Câu 1. Trong số các chất sau: Cl2, HCl, F2, SO2, FeO, HNO3. Có bao nhiêu chất vừa đóng vai trò là chất oxi hóa, vừa đóng vai trò là chất khử?
Đáp án: 4
Các nguyên tố có số oxi hóa nằm giữa các số oxi hóa còn lại → vừa có tính khử, vừa có tính oxi hóa: Cl2, HCl, SO2, FeO.
- Cl có các số oxi hóa: -1, 0, +1, +3, +5, +7. Cl2 có số oxi hóa 0 nằm giữa các số oxi hóa còn lại.
- Phân tử HCl: thể hiện tính oxi hóa khi phản ứng tạo ra H2, thể hiện tính khử khi phản ứng tạo ra Cl2
- F có các số oxi hóa 0, -1. F2 có số oxi hóa 0 nên chỉ thể hiện tính oxi hóa.
- S có các số oxi hóa: -2, 0, +4, +6. S/SO2 có số oxi hóa +4 nằm giữa các số oxi hóa còn lại.
- Fe có các số oxi hóa: 0, +2, +8/3, +3. Fe/FeO có số oxi hóa +2 nằm giữa các số oxi hóa còn lại.
- N có các số oxi hóa: -3, 0, +1, +2, +3, +4, +5. N/HNO3 có số oxi hóa +5 nên chỉ có tính oxi hóa.
Câu 2. Hệ số của HNO3 trong phương trình: aAl + bHNO3 → cAl(NO3)3 + dNO2 + eH2O là bao nhiêu?
Đáp án: 6
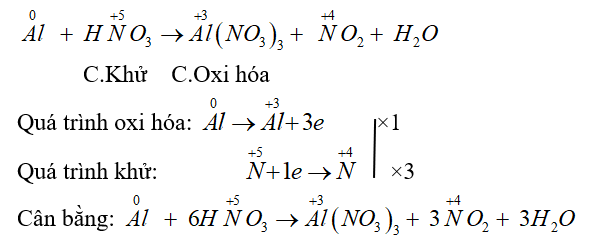
Câu 3. Có bao nhiêu phản ứng oxi hóa – khử trong các phản ứng sau
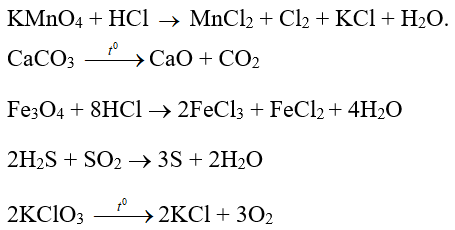
Đáp án: 3
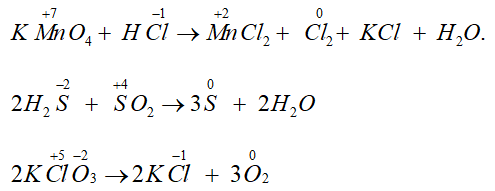
Là các phản ứng oxi hóa - khử. Vì có sự thay đổi số oxi hóa của một số nguyên tố trong phản ứng.
Câu 4. Trong phản ứng: KMnO4 + HCl → MnCl2 + Cl2 + KCl + H2O.
Số phân tử HCl đóng vai trò chất khử bằng k lần tổng số phân tử HCl tham gia phản ứng. Giá trị của k là bao nhiêu?
Đáp án: 5/8
Cân bằng phản ứng ta có: 2KMnO4 + 16HCl → 2MnCl2 + 5Cl2 + 2KCl + 8H2O.

Do đó: k = 10/16 = 5/8
Câu 5. Cho dãy gồm các phân tử và ion: Zn, S, SO2, Fe2+, Cu2+, HCl, SO2-3 . Có bao nhiêu phân tử và ion trong dãy vừa có tính khử, vừa có tính oxi hóa?
Đáp án: 5
Tương tự câu 1 ta có dãy các chất và ion vừa có tính khử, vừa có tính oxi hóa là: S, SO2, Fe2+, HCl, SO2-3
Câu 6. Cho các phản ứng sau:
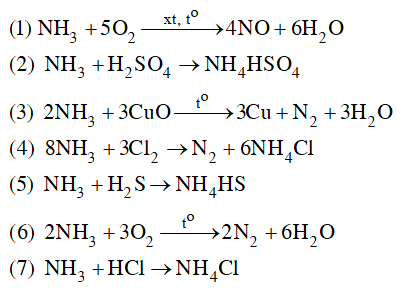
Có bao nhiêu phản ứng trong đó NH3 không đóng vai trò là chất khử?
Đáp án: 3
Ba phương trình (2), (5), (7) không có sự thay đổi số oxi hóa trước và sau phản ứng nên không phải là phản ứng oxi hóa khử → NH3 không đóng vai trò là chất khử.
Câu 7. Hoà tan hoàn toàn 11,2 gam Fe bằng dung dịch H2SO4 đặc, thu được V lít SO2 (ở nhiệt độ 250C và áp suất 1 bar). Tính giá trị của V?
Đáp án: 7,437 (lít)
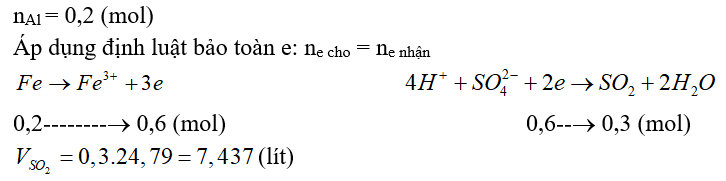
Câu 8. Hoà tan hoàn toàn 1,95g Zn bằng dung dịch HNO3, thu được x mol khí NO (sản phẩm khử duy nhất của N+5). Gía trị của x là bao nhiêu?
Đáp án: 0,02

Câu 9. Cho 18,4 gam hỗn hợp Zn và Al tác dụng với lượng dư dung dịch H2SO4 đặc, nóng thu được 12,395 lít khí SO2 (ở đkc, là sản phẩm khử duy nhất). Có bao nhiêu phần trăm khối lượng của Zn trong hỗn hợp ban đầu?
Đáp án: 70,65%
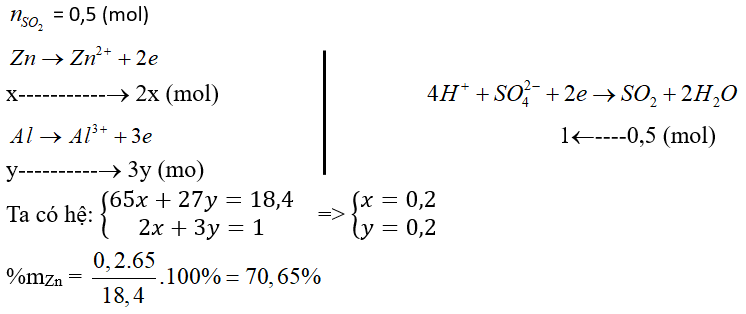
Câu 10. Hoà tan hoàn toàn 12 gam hỗn hợp Fe, Cu (tỉ lệ mol 1:1) bằng acid HNO3, thu được V lít (ở đkc) hỗn hợp khí X (gồm NO và NO2) và dung dịch Y (chỉ chứa hai muối và acid dư). Tỉ khối của X đối với H2 bằng 19. Giá trị của V là bao nhiêu?
Đáp án: 6,1975 (lít)

