Trắc nghiệm Đúng sai Trả lời ngắn Hóa 10 Bài 10: Liên kết cộng hóa trị
Tổng hợp 20 câu Trắc nghiệm Đúng sai Trả lời ngắn Hóa 10 Bài 10: Liên kết cộng hóa trị có đáp án chi tiết bám sát chương trình học Sách mới năm học 2024-2025
Phần 1. Trắc nghiệm Đúng Sai
Câu 1. Methane thường được sử dụng để làm nhiên liệu trong các lò nướng, máy nước nóng, lò nung, xe ôtô do quá trình đốt cháy methane (CH4) trong oxygen tỏa ra lượng nhiệt lớn. Methane ở dạng khí nén được dùng làm nhiên liệu cho ôtô, xe máy,… do đặc tính thân thiện với môi trường. (Cho ZC = 6, ZH = 1)
A. Số cặp electron chung giữa nguyên tử carbon và các nguyên tử hydrogen là 4.
B. Trong phân tử CH4 chứa liên kết cộng hóa trị không phân cực.
C. Phân tử CH4 có công thức Lewis và công thức cấu tạo giống nhau.
D. Phân tử CH4 chỉ chứa các liên kết đơn.
A. đúng
C. đúng
D. đúng
Câu 2. Ozone (O3) là một loại khí có tính oxi hóa mạng, phân tử gồm ba nguyên tử oxygen. Ozone xuất hiện ở tầng đối lưu và tầng bình lưu của khí quyển. Tùy thuộc vào vị trí của ozone trong các tầng trên mà nó ảnh hưởng đến sự sống trên Trái Đất theo các cách tốt, xấu khác nhau.
A. Phân tử ozone có sự hiện diện liên kết cho – nhận
B. Ozone là một phân tử phân cực nên tan trong nước nhiều hơn O2.
C. Liên kết π trong phân tử O3 được hình thành tự sự xen phủ trục của hai orbital p.
D. Mỗi nguyên tử O còn hai cặp electron hoá trị riêng.
A. đúng
B. đúng
Câu 3. Các nguyên tố phổ biến thuộc nhóm halogen (VIIA) trong bảng tuần hoàn các nguyên tố hóa học gồm: F (Z = 9), Cl (Z = 17), Br (Z = 35) và I (Z = 53). Các hydrogen halide có dạng là HX. Cho biết năng lượng liên kết H-F, H-I, H-Br và H-Cl lần lượt là 565 kJ/mol, 295 kJ/mol, 363 kJ/mol, 427 kJ/mol
A. Khi đun nóng, HI bị phân huỷ (thành H2 và I2) ở nhiệt độ thấp hơn so với HBr (thành H2 và Br2).
B. Phản ứng của Cl2 với H2 xảy ra dễ hơn so với phản ứng của Br2 với H2.
C. Khi đun nóng, HCl bị phân huỷ (thành H2 và Cl2) ở nhiệt độ thấp hơn so với HBr (thành H2 và Br2).
D. Độ bền liên kết: HCl < HBr < HI < HF.
A. đúng
B. đúng
Câu 4. Cho bảng số liệu sau:
Nguyên tử |
H |
O |
S |
|---|---|---|---|
Độ âm điện |
2,20 |
3,44 |
2,58 |
A. Trong phân tử H2O và phân tử H2S chỉ có các liên kết cộng hóa trị.
B. Số liên kết trong phân tử H2O bằng số liên kết trong phân tử H2S.
C. Liên kết O-H trong phân tử H2O kém phân cực hơn liên kết S-H trong phân tử H2S.
D. Phân tử H2O và phân tử H2S đều là những phân tử phân cực
A. đúng
B. đúng
D. đúng
Câu 5. Cho số hiệu các nguyên tử của H, F và N lần lượt là 1, 9 và 7.
A. Sự tạo liên kết trong các phân tử NH3 và F2 theo kiểu xen phủ của các orbital cùng loại.
B. Cả hai phân tử NH3 và F2 đều chứa liên kết cộng hóa trị không phân cực.
C. Trong phân tử N2 có chứa 1 liên kết σ và 2 liên kết π.
D. Các chất HF, NH3 đều tan tốt trong nước.
C. đúng
D. đúng
Câu 6. Cho sơ đồ biểu diễn sự hình thành liên kết trong phân tử khí carbon dioxide.
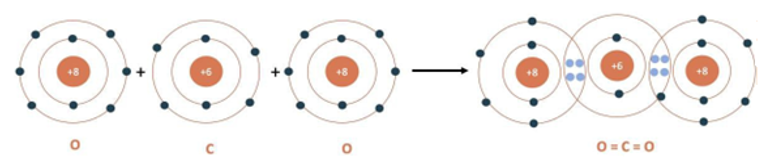
A. Liên kết giữa nguyên tử O và C là liên kết phân cực.
B. Phân tử carbon dioxide số liên kết σ và liên kết π lần lượt là 2 và 2.
C. Phân tử CO2 không phân cực do tổng momen lưỡng cực trong phân tử bằng không
D. Giữa nguyên tử C với mỗi nguyên tử O có 2 cặp electron chung
A. đúng
B. đúng
C. đúng
D. đúng
Câu 7. Năng lượng liên kết và độ dài liên kết của C – C, C = C, và C ≡ C trong các phân tử C2H6, C2H4, và C2H2 được cho bởi bảng sau:
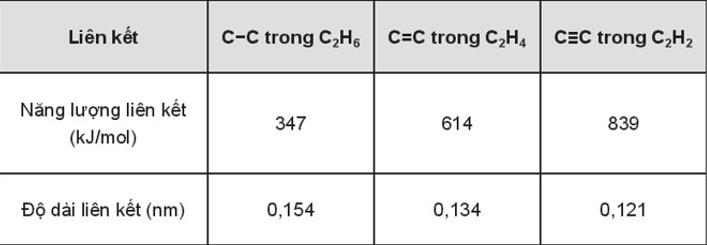
A. Chiều dài liên kết tỉ lệ nghịch với năng lượng liên kết giữa các nguyên tử carbon trong các hydrocarbon
B. Độ bền liên kết tăng theo thứ tự C ≡ C, C = C, C-C
C. Liên kết giữa các nguyên tử C trong các hydrocarbon trên là liên kết cộng hoá trị không phân cực.
D. Các hydrocarbon C2H6, C2H4, C2H2 đều tan tốt trong các dung môi phân cực.
A. đúng
C. đúng
Câu 8. Cho các hình biểu diễn sự xen phủ orbital nguyên tử để tạo liên kết hóa học sau:

A. Chỉ có các AO có hình dạng giống nhau mới xen phủ với nhau để tạo liên kết.
B. Khi hình thành liên kết cộng hoá trị giữa hai nguyên tử, luôn có một liên kết σ.
C. Có hai kiểu xen phủ hình thành liên kết là xen phủ trục và xen phủ bên.
D. Vùng xen phủ của sự xen phủ trục nằm trên đường nối tâm của hai nguyên tử.
B. đúng
C. đúng
D. đúng
Câu 9. "Nước" là tên trạng thái lỏng của H2O ở điều kiện tiêu chuẩn về nhiệt độ và áp suất. Nước bao phủ 71% bề mặt Trái đất, chủ yếu ở các biển và đại dương. Nước đóng một vai trò quan trọng trong nền kinh tế thế giới. Khoảng 70% lượng nước ngọt mà con người sử dụng được dùng cho nông nghiệp.[10] Đánh bắt cá ở các vùng nước mặn và nước ngọt là nguồn cung cấp thực phẩm chính cho nhiều nơi trên thế giới. Cho giá trị độ âm điện của H là 2,20 và O là 3,44.
A. Liên kết H – O là liên kết cộng hoá trị phân cực.
B. Cặp electron dùng chung trong liên kết H – O phân bố đều giữa hai nguyên tử.
C. Nguyên tử O còn hai cặp electron hoá trị riêng.
D. H2O là dung môi phân cực có thể hòa tan các chất phân cực.
A. đúng
C. đúng
D. đúng
Câu 10. Cho cấu hình electron hóa trị của 3 nguyên tố sau: X (ns1), Y (ns2np1), Z (ns2np5) (n = 3)
A. Liên kết giữa Z và Y là liên kết cộng hoá trị có cực.
B. Liên kết giữa Z và X là liên kết cộng hoá trị.
C. Phân tử Y2 được hình thành thừ sự xen phủ orbital p - p.
D. Phân tử XZ tan trong nước tốt hơn phân tử Y2.
A. đúng
C. đúng
D. đúng
Phần 2. Câu hỏi Trả lời ngắn
Câu 1. Có bao nhiêu hợp chất cộng hóa trị trong dãy các chất sau: NH3, CaO, KCl, CH4, CO2, H2O?
Đáp án: 4
Hợp chất cộng hóa trị: NH3, CH4, CO2, H2O.
Câu 2. Cho số hiệu của nguyên tố S và O lần lượt là 16 và 8. Biết rằng hóa trị của nguyên tố S trong phân tử H2SO4 bằng tổng số liên kết σ và liên kết π mà nguyên tử S tạo thành khi liên kết với các nguyên tử xung quanh. Trong phân tử H2SO4 , nguyên tử S không liên kết với nguyên tử H mà liên kết với 4 nguyên tử O. Từ đó viết được công thức Lewis phù hợp của phân tử H2SO4 với hóa trị của S là . Giá trị của n là bao nhiêu?
Đáp án: 6
Công thức Lewis của H2SO4:
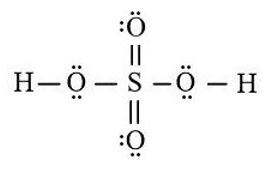
Tổng số liên kết σ và liên kết π mà nguyên tử S tạo thành khi liên kết là 6.
Câu 3. Biết phân tử BF3 có cấu trúc phẳng, phân tử CCl4 có cấu trúc hình tứ diện đều. Hãy cho biết có bao nhiêu phân tử phân cực trong hình dưới đây?
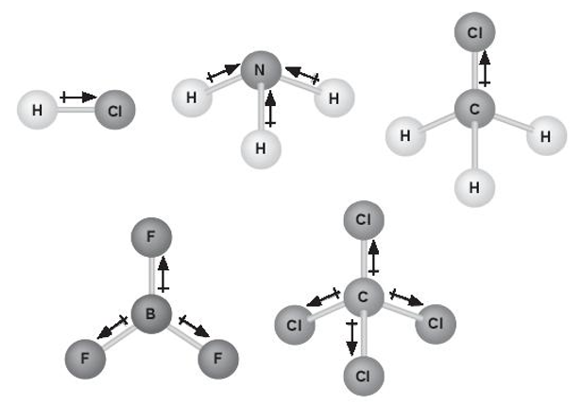
Đáp án: 3
Ba phân tử đầu: HCl, NH3, CH3Cl đều là các phân tử phân cực, do tổng moment lưỡng cực khác không
- Hai phân tử sau: BF3, CCl4 đều là các phân tử không phân cực do tổng moment lưỡng cực triệt tiêu.
Câu 4. Cho biết năng lượng của một số liên kết ở điều kiện chuẩn: H-S là 368 kJ/mol và H - O là 464 kJ/mol. Tính tổng năng lượng liên kết trong mỗi phân tử H2S và H2O.
Đáp án: 736 và 928 kJ/mol
Tổng năng lượng liên kết là 2EH – X với X là S, O.
Tổng năng lượng liên kết trong phân tử H2S là: 2 × 368 = 736 (kJ mol-1)
Tổng năng lượng liên kết trong phân tử H2O là: 2 × 464 = 928 (kJ mol-1)
Câu 5. Tổng số cặp electron dùng chung giữa các nguyên tử trong phân tử ethylene (C2H4) là bao nhiêu?
Đáp án: 6
Công thức electron của C2H4
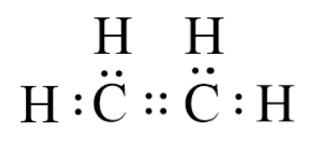
Câu 6. Dưới đây là biểu đồ tương tác của hai nguyên tử hydrogen ở thể khí so với khoảng cách hạt nhân giữa chúng:
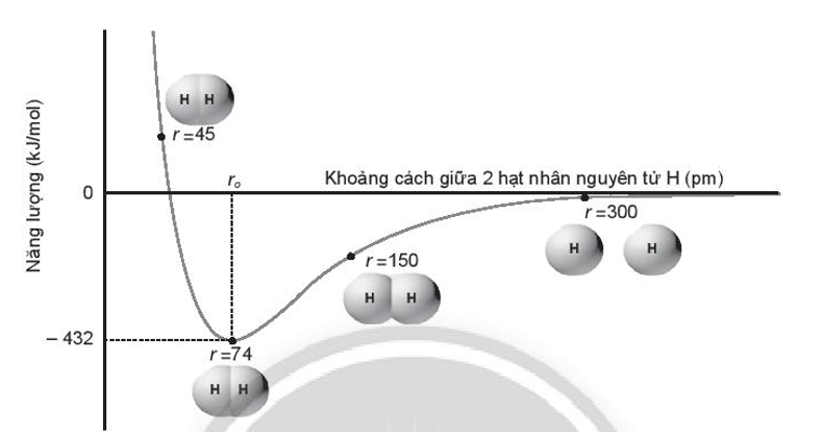
Cho biết năng lượng liên kết của phân tử hydrogen (H2) và độ dài liên kết H – H là bao nhiêu?
Đáp án: 432 kJ/mol và 74 pm
Trên biểu đồ, năng lượng tối thiểu đại diện cho độ bền liên kết và khoảng cách ro tại mức năng lượng tối thiểu gọi là độ dài liên kết. Do đó phân tử H2 có năng lượng liên kết là 432 kJ/mol và có độ dài liên kết H – H là 74 pm.
Câu 7. Cho biết trong các phân tử sau MgCl2, AlCl3, HBr, O2, H2 và NH3. Dựa vào giá trị độ âm điện, cho biết có bao nhiêu phân tử có liên kết cộng hóa trị phân cực?
Nguyên tử |
Mg |
Al |
H |
N |
Cl |
Br |
O |
|---|---|---|---|---|---|---|---|
Độ âm điện |
1,31 |
1,61 |
2,20 |
3,04 |
3,16 |
2,96 |
3,44 |
Đáp án: 3
Các phân tử : AlCl3, HBr và NH3.
Câu 8. Cho công thức Lewis của các phân tử sau:
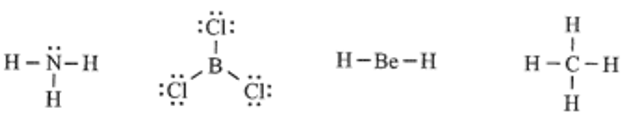
Số phân tử mà nguyên tử trung tâm không thoả mãn quy tắc octet là bao nhiêu?
Đáp án: 1
Câu 9. Một nguyên tử X có tổng số electron ở các phân lớp s là 6 và tổng số electron ở lớp ngoài cùng cũng là 6. Phân tử hợp chất tạo thành giữa X và O có dạng XO2. Trong phân tử XO2 có bao nhiêu cặp electron chung?
Đáp án: 3
X có cấu hình e là 1s22s22p63s23p4 => X là S

=> có 3 cặp electron chung
Câu 10. Cho chất hữu cơ A có công thức cấu tạo sau: CH3–C≡C–CH3. Số liên kết σ trong phân tử A?
Đáp án: 10
