Trắc nghiệm Đúng sai Trả lời ngắn Hóa 10 Bài 9: Liên kết ion
Tổng hợp 20 câu Trắc nghiệm Đúng sai Trả lời ngắn Hóa 10 Bài 9: Liên kết ion có đáp án chi tiết bám sát chương trình học Sách mới năm học 2024-2025
Phần 1. Trắc nghiệm Đúng Sai
Câu 1. Cho 2 ion Sodium (11Na+) và Oxide (8O2-)
A. Hợp chất tạo thành giữa Na+ và O2– là hợp chất ion.
B. Hợp chất tạo thành có công thức hóa học là NaO.
C. Lực tương tác giữa Na+ và O2– là lực tĩnh điện.
D. Trong điều kiện thường, hợp chất tạo thành tồn tại ở thể rắn.
A. đúng
C. đúng
D. đúng
Câu 2. Nguyên tố X tích lũy trong các tế bào thực vật nên rau và trái cây tươi là nguồn cung cấp tốt nguyên tố X cho cơ thể. Các nghiên cứu chỉ ra khẩu phần ăn chứa nhiều X có thể giảm nguy cơ cao huyết áp và đột quỵ. Nguyên tố Z được dùng chế tạo dược phẩm, phẩm nhuộm và chất nhạy với ánh sáng. Nguyên tử X chỉ có 7 electron trên phân lớp s; còn nguyên tử Z chỉ có 17 electron trên phân lớp p.
A. Công thức hóa học của hợp chất tạo bởi X và Z là XZ.
B. Hợp chất tạo bởi X và Z không dẫn điện.
C. Hợp chất XZ là một muối được sử dụng rộng rãi như thuốc chống co giật và an thần.
D. Tổng số hạt mang điện dương của 2 nguyên tử X và Z là 54
A. đúng
C. đúng
D. đúng
Câu 3. Potassium iodide (KI) được sử dụng như một loại thuốc long đờm, giúp làm lỏng và phá vỡ chất nhầy trong đường thở, thường dùng cho các bệnh nhân hen suyễn, viêm phế quản mãn tính. Trong trường hợp bị nhiễm phóng xạ, KI còn giúp ngăn tuyến giáp hấp thụ iodide phóng xạ, bảo vệ và làm giảm nguy cơ ung thu tuyến giáp.
A. Trong phân tử KI, các nguyên tử K và I đều đã đạt được cấu hình bền của khí hiếm gần nhất.
B. Liên kết trong phân tử KI là liên kết cộng hoá trị
C. Hợp chất được tạo thành từ ion K- và ion I+
D. Hợp chất dễ tan trong nước tạo thành dung dịch dẫn điện.
A. đúng
D. đúng
Câu 4. Cho mô hình tinh thể NaCl như hình dưới:
A. Để lắp được mô hình trên cần 27 khối cầu gồm (Cl- và Na+) và 54 thanh nối
B. Số ion chloride (Cl-) bao quanh gần nhất với ion sodium (Na+) là 6
C. Tinh thể NaCl có cấu trúc của hình lập phương
D. Ở điều kiện thường, NaCl tồn tại dạng tinh thể rắn, cứng, không tan trong nước và có nhiệt độ nóng chảy khá cao
A. đúng
B. đúng
C. đúng
Câu 5. Cho hợp chất sodium oxide (Na2O)?
A. Trong phân tử Na2O, các ion Na+ và ion O2- đều đạt cấu hình electron bền vững của khí hiếm neon.
B. Phân tử Na2O tạo bởi lực hút tĩnh điện giữa hai ion Na+ và một ion O2-.
C. Là chất rắn trong điều kiện thường.
D. Không tan trong nước, chỉ tan trong dung môi không phân cực như benzene, carbon tetrachloride,…
A. đúng
B. đúng
C. đúng
Câu 6. Tính chất của hợp chất ion
A. Tồn tại ở thể khí trong điều kiện thường.
B. Có nhiệt độ nóng chảy và nhiệt độ sôi cao.
C. Liên kết ion thường hình thành giữa kim loại điển hình và phi kim điển hình.
D. Hợp chất ion tan tốt trong dung môi không phân cực.
B. đúng
C. đúng
Câu 7. X có cấu hình e ở phân lớp ngoài cùng là 4s1. Y có 11 electron ở phân lớp p.
A. X là phi kim, Y là kim loại.
B. Liên kết giữa X và Y là liên kết ion.
C. Hợp chất tạo bởi X và Y là X2Y.
D. X tạo được anion, Y tạo được cation.
B. đúng
Câu 8. Sodium sulfide (Na2S) là một hợp chất hóa học được sử dụng trong ngành công nghiệp giấy và bột giấy, xử lí nước, công nghiệp dệt may và các quá trình sản xuất hóa chất khác nhau như sản xuất cao su, thuốc nhuộm sulfur và thu hồi dầu,… Điều thú vị là sodium sulfide đã được chứng minh là có vai trò trong bảo vệ tim mạch, chống lại chứng thiếu máu cục bộ ở tim và giúp bảo vệ phổi, chống lại tổn thương phổi do máy thở.
A. Mỗi nguyên tử Na đã nhường 1 electron, nguyên tử S nhận 2 electron từ nguyên tử Na để hình thành hợp chất ion Na2S
B. Bán kính ion Na+(Z= 11) > bán kính ion S2- (Z= 16)
C. Ion Sodium và ion sulfide đều có cấu hình bền vững của nguyên tử khí hiếm gần nhất với nguyên tố tạo thành ion đó trong bảng tuần hoàn
D. Tổng số hạt mang điện trong phân tử Na2S là 76 hạt.
A. đúng
C. đúng
D. đúng
Câu 9. Hợp chất X có công thức là A2B có tổng số hạt (p, n, e) là 92, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 28. Nguyên tử nguyên tố A có số proton nhiều hơn so với nguyên tử nguyên tố B là 3.
A. Hợp chất X có công thức là A2B là hợp chất ion
B. Hợp chất tạo thành từ ion A+ và ion B2-
C. Ion A+ và B2- có cùng cấu hình electron
D. Hợp chất A2B tan trong nước tạo dung dịch làm quỳ tím chuyẻn sang màu xanh
A. đúng
B. đúng
C. đúng
D. đúng
Câu 10. Khi đun nóng dung dịch sodium chloride bão hòa, thu được tinh thể sodium chloride khan. Sau đó, nung nóng đến khoảng 800 °C thì tinh thể sodium chloride chảy lỏng.
A. Quá trình hình thành tinh thể sodium chloride ở trên được gọi là sự kết tinh.
B. Quá trình hình thành tinh thể sodium chloride ở trên là quá trình sắp xếp lại các ion Na+, Cl- từ chuyển động tự do thành cấu trúc có trật tự trong tinh thể.
C. Trong tinh thể sodium chloride, xung quanh 1 ion Na+ có 6 ion Cl- gần nhất.
D. Tinh thể sodium chloride nóng chảy ở khoảng 800 °C, chứng tỏ lực liên kết giữa các ion trong tinh thể là yếu.
A. đúng
B. đúng
C. đúng
Phần 2. Câu hỏi Trả lời ngắn
Câu 1. Cho các chất sau: NaCl, H2O, K2O, BaCl2, CaF2, HCl, NH4NO3. Số phân tử có liên kết ion là ?
Đáp án: 5
NaCl, K2O, BaCl2, CaF2, NH4NO3.
Câu 2. Để đạt quy tắc octet, nguyên tử Na (Z=11) đã nhường bao nhiêu electron?
Đáp án: 1
Na → Na + + 1e
Câu 3. Trong hợp chất ion XY (X là kim loại, Y là phi kim), số electron của cation bằng số electron của anion và tổng số electron trong XY là 20. Biết trong mọi hợp chất, Y chỉ có một mức oxi hóa duy nhất. Số hạt mang điện trong nguyên tử X là ?
Đáp án: 22
Gọi số e của X là e1, số e của Y là e2
e1 + e2 = 20
e1 – 1 = e2 + 1
suy ra : e1 = 11, e2 = 9
Số hạt mang điện của X là 11 * 2 = 22
Câu 4. Trong đời sống muối ăn (NaCl) và các gia vị, phụ gia C5H8NO4Na: (bột ngọt) C7H5O2Na (Chất bảo quản thực phẩm) đều có chứa ion sodium. Hiệp hội Tim mạch Hoa Kỳ khuyến cáo lượng ion sodium mỗi ngày được nạp vào cơ thể mỗi người cần thấp hơn 2300mg để bảo vệ tim mạch và thận. Nếu trung bình mỗi ngày một người dùng tổng cộng 5 gam muối ăn; 0,5 gam bột ngọt; 0,05 gam chất bảo quản thì lượng sodium tiêu thụ thấp hơn mức cho phép là bao nhiêu mg ?
Đáp án: 258
Lượng sodium người đó tiêu thụ một ngày là:
[(5 x 23) : 58,5] + [0,5 x 23) : 169] + [0,05 x 23) : 144] = 2,042 gam = 2042 mg < 2300 mg
=> Người đó tiêu thụ lượng sodium thấp hơn mức cho phép là.
2300 mg - 2042 mg = 258 mg
Câu 5. Cho các ion: Li+, Ca2+, Al3, F–, O2–, PO3-4 . Có thể viết được tất cả bao nhiêu hợp chất ion tạo thành từ các ion đã cho (tạo nên từ một loại cation và một loại anion). Cho biết tổng điện tích của các ion trong hợp chất bằng 0.
Đáp án: 9
LiF; Li2O; Li3PO4; CaF2; CaO; Ca3(PO4)2; AlF3; Al2O3; AlPO4
Câu 6. Theo nghiên cứu của Đại học Harvard vào năm 2013, trẻ em sinh sống tại những khu vực có nguồn nước bị nhiễm Fluorine có chỉ số IQ trung bình sẽ thấp hơn so với những trẻ em sống tại vùng kháC. Anion F- (fluoride) có độc tính mạnh với hệ thần kinh. Với lượng tương đối thấp: 0,2 gam ion F- trên cơ thể có trọng lượng 70 kg có thể gây tử vong. Tuy nhiên, sự có mặt của anion fluoride lại giúp men răng chắc khỏe và chống chọi các bệnh về sâu răng, vì vậy anion fluoride được thêm vào nước uống đóng chai với nồng độ với nồng độ 1mg ion F- trên 1L nước và bổ sung một lượng nhỏ dưới dạng muối sodium fluoride (NaF) trong kem đánh răng. Một bạn học sinh nặng khoảng 70kg sử dụng loại nước chứa ion F- với lượng 1mg/1L để giúp men răng chắc khỏe, chống sâu răng. Sau khi đọc thông tin về độc tính của ion F-, bạn học sinh rất lo lắng. Hãy tính xem với thể tích nước mà bạn học sinh này uống một ngày là bao nhiêu lít thì ion F- có trong nước đạt đến mức có thể gây độc tính?
Đáp án: 200
1mg/ 1L là liều lượng không độc
0,2 g/ 70 kg là liều lượng đến mức F- gây độc tính ở đâu đấy ?
0,2 g = 200 mg tương ứng 200L nước
Vậy một người 70kg uống 200L nước chứa F- mới có khả năng nhiễm độc fluoride
Câu 7. Theo hiệp hội nha khoa Hoa Kỳ, một người trưởng thành nên bổ sung 3,0 mg F- mỗi ngày dưới dạng muối sodium fluoride (NaF) để ngăn ngừa sâu răng. Lượng NaF không gây độc cho cơ thể khi ở mức 3,19.10-2 gam/ 1 kg cơ thể. Một mẫu kem đánh răng chứa 0,28% NaF, hãy tính khối lượng mẫu kem đánh răng mà một người nặng 75 kg có thể nuốt nhưng không gây độc tính với cơ thể?
Đáp án: 854,46
3,19.10-2 x 75 = 2,3925 g
mkem đánh răng= 2,3925.100/0,28 = 854,464 gam.
Câu 8. Nguyên tử X có có tổng số hạt cơ bản là 60 và thuộc nhóm IIA. Nguyên tử Y có tổng số hạt cơ bản là 52 và thuộc nhóm VIIA. Tính tổng số hạt mang điện âm trong phân tử hợp chất tạo bởi X và Y ?
Đáp án: 54
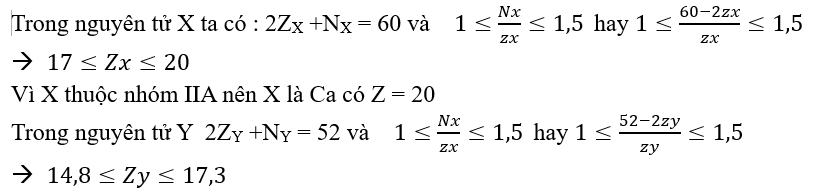
Vì Y thuộc nhóm VIIA nên X là Cl có Z = 17. Hợp chất tạo bởi X và Y có công thức CaCl2 có tổng số hạt mang điện âm là : 20 + (17.2) = 54
Câu 9. Nguyên tử nguyên tố X có mức năng lượng cao nhất ở phân lớp 3p. Nguyên tử nguyên tố Y cũng có mức năng lượng ở phân lớp 3p và có tổng số electron ở lớp ngoài cùng là 1. Biết số hạt mang điện dương trong hạt nhân nguyên tử nguyên tố Y nhiều hơn trong nguyên tố X là 3 hạt. Tổng số e độc thân của 2 nguyên tử ở trạng thái cơ bản là?
Đáp án: 3
Y có electron ở mức năng lượng 3p và có một electron ở lớp ngoài cùng
→ Cấu hình electron của Y là 1s22s22p63s23p64s1 → Y là kim loại.
X có electron ở mức năng lượng cao nhất là 3p theo bài ra thì X kém Y 2 electron
→ Cấu hình electron của X là 1s22s22p63s23p5 → X là phi kim.
Câu 10. Hợp chất X có công thức là A2B có tổng số hạt (p, n, e) là 92, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 28. Nguyên tử nguyên tố A có số proton nhiều hơn so với nguyên tử nguyên tố B là 3. Số hạt mang điện của nguyên tử A là ?
Đáp án: 22
Gọi các hạt trong nguyên tử A là n1, e1, p1
Các hạt trong nguyên tử B là n2, e2, p2
Theo bài ra , ta có: 4p1 + 2n1 + 2p2 + n2 = 92
4p1 + 2p2 – 2n1 – n2 = 28
p1 – p2 = 3
Suy ra p1 = 11, p2 = 8
Vậy số hạt mang điện của A là 11+ 11 = 22
