Soạn KHTN 8 Bài 6: Tính theo phương trình hóa học
Hướng dẫn Soạn KHTN 8 Bài 6: Tính theo phương trình hóa học ngắn gọn, hay nhất theo chương trình Sách mới.
Bài 6: Tính theo phương trình hóa học
Lý thuyết Khoa học tự nhiên 8 Kết nối tri thức Bài 6: Tính theo phương trình hóa học
Sơ đồ tư duy Khoa học tự nhiên 8 Kết nối tri thức Bài 6: Tính theo phương trình hóa học
Mở đầu trang 28 Bài 6 KHTN 8: Bằng cách nào có thể tính được lượng chất tham gia và lượng chất sản phẩm trong quá trình sản xuất?
Trả lời:
- Dựa vào phương trình hoá học, khi biết lượng một chất đã phản ứng hoặc lượng chất tạo thành tính được lượng các chất còn lại.
Câu hỏi 1 trang 29 KHTN 8: Ví dụ: Hoà tan hết 0,65 gam Zn trong dung dịch HCl 1 M, phản ứng xảy ra như sau:
Zn + 2HCl → ZnCl2 + H2
Tính thể tích khí hydrogen thu được trong ví dụ trên ở 25 oC, 1 bar.
Trả lời:
Số mol Zn tham gia phản ứng:
nZn=0,65/65=0,01(mol)
Theo phương trình hoá học:
1 mol Zn tham gia phản ứng sẽ thu được 1 mol H2.
Vậy 0,01 mol Zn tham gia phản ứng sẽ thu được 0,01 mol H2.
Thể tích khí hydrogen thu được ở 25oC, 1 bar (tức điều kiện chuẩn) là:
V = 0,01 . 24,79 = 0,2479 lít.
Câu hỏi 2 trang 29 KHTN 8: Khi cho Mg tác dụng với dung dịch H2SO4 loãng thì xảy ra phản ứng hoá học như sau:
Mg + H2SO4 → MgSO4 + H2
Sau phản ứng thu được 0,02 mol MgSO4. Tính thể tích khí H2 thu được ở 25oC, 1 bar.
Trả lời:
Ta có nMgSO4 = 0,02 mol
Theo phương trình hoá học ta có 1 mol Mg phản ứng sinh ra 1 mol MgSO4 và 1 mol H2
Vậy 0,02 mol MgSO4 sinh ra cũng sẽ có 0,02 mol H2 được sinh ra sau phản ứng
V H2 = 0,02 x 24,79 = 0,4958 mol
Câu hỏi trang 29 KHTN 8: Khi nung nóng KClO3 xảy ra phản ứng hoá học sau (phản ứng nhiệt phân):
2KClO3 to→ 2KCl + 3O2
Biết rằng hiệu suất phản ứng nhỏ hơn 100%.
Hãy chọn các từ/cụm từ (lớn hơn, nhỏ hơn, bằng) phù hợp với nội dung còn thiếu trong các câu sau đây:
- Khi nhiệt phân 1 mol KClO3 thì thu được số mol O2 … (1) … 1,5 mol.
- Để thu được 0,3 mol O2 thì cần số mol KClO3 … (2) … 0,2 mol.
Trả lời:
- Khi nhiệt phân 1 mol KClO3 thì thu được số mol O2 nhỏ hơn 1,5 mol.
- Để thu được 0,3 mol O2 thì cần số mol KClO3 lớn hơn 0,2 mol.
Câu hỏi trang 30 KHTN 8: Nung 10 gam calcium carbonate (thành phần chính của đá vôi), thu được khí carbon dioxide và m gam vôi sống. Giả thiết hiệu suất phản ứng là 80%, xác định m
Trả lời:
Số mol CaCO3: nCaCO3 = 10/100 = 0,1 (mol)
Phương trình hoá học: CaCO3 to→ CaO + CO2
Theo phương trình hoá học:
1 mol CaCO3 tham gia phản ứng thu được 1 mol CaO.
Vậy 0,1 mol CaCO3 tham gia phản ứng thu được 0,1 mol CaO.
Khối lượng CaO thu được theo lí thuyết là: mLT = 0,1.56 = 5,6 gam.
Do hiệu suất phản ứng là 80% nên khối lượng CaO thu được theo thực tế là:
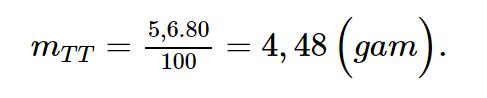
>>> Xem toàn bộ: Soạn KHTN 8 Kết nối tri thức
-------------------------------------
Trên đây Toploigiai đã cùng các bạn Trả lời câu hỏi KHTN 8 Kết nối tri thức Bài 6: Tính theo phương trình hóa học trong bộ SGK Kết nối tri thức theo chương trình sách mới. Chúc các bạn học tốt!
