Lý thuyết KHTN 8 Bài 4 Kết nối tri thức
Tóm tắt Lý thuyết Khoa học tự nhiên 8 Kết nối tri thức Bài 4. Dung dịch và nồng độ theo chương trình Sách mới ngắn gọn nhất. Tổng hợp lý thuyết Khoa học tự nhiên 8 trọn bộ chi tiết, đầy đủ.
Bài 4. Dung dịch và nồng độ
Soạn KHTN 8 Kết nối tri thức Bài 4: Dung dịch và nồng độ (trang 20)
I. Dung dịch, chất tan và dung môi
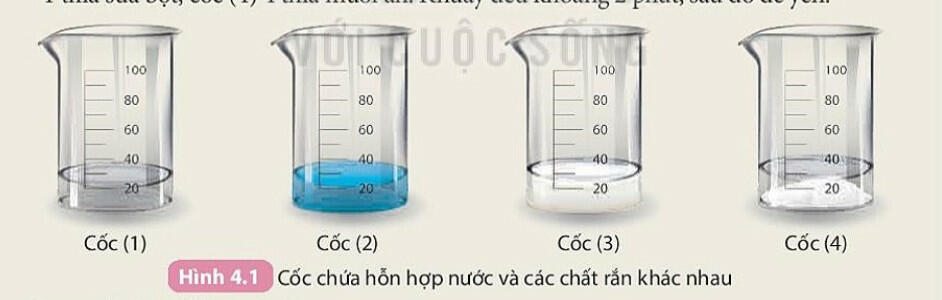
- Dung dịch là hỗn hợp đồng nhất của chất tan và dung môi.
- Dung môi thường là nước ở thể lỏng, chất tan có thể ở thể rắn, lỏng hoặc khí.
- Dung dịch chưa bão hoà là dung dịch có thể hoà tan thêm chất tan ở nhiệt độ, áp suất nhất định, còn dung dịch bão hoà là dung dịch không thể hoà tan thêm chất tan.
II. Độ tan
- Khả năng tan của các chất trong cùng một dung môi khác nhau dù ở cùng điều kiện về nhiệt độ và áp suất.
- Những chất tan tốt cần lượng lớn chất tan để tạo dung dịch bão hoà, còn những chất tan kém chỉ cần lượng nhỏ chất tan đã thu được dung dịch bão hoà.
- Độ tan của một chất trong nước là số gam chất đó hoà tan trong 100 gam nước để tạo thành dung dịch bão hoà ở nhiệt độ, áp suất xác định.
- Độ tan của một chất trong nước được tính bằng công thức: S = (mct/mnước) x 100, trong đó S là độ tan, đơn vị g/100 g nước; mct là khối lượng chất tan, đơn vị là gam (g); mnước là khối lượng nước, đơn vị là gam (g).
III. Nồng độ dung dịch
- Nồng độ dung dịch là đại lượng được sử dụng để định lượng một dung dịch đặc hay loãng. Có hai loại nồng độ dung dịch thường dùng là nồng độ phần trăm và nồng độ mol.
- Nồng độ phần trăm:
Nồng độ phần trăm (C%) của một dung dịch cho biết số gam chất tan có trong 100 gam dung dịch. Nồng độ phần trăm được xác định bằng công thức:
C% = (mct/ mdd) x 100%
Trong đó: C% là nồng độ phần trăm của dung dịch, đơn vị %; mct là khối lượng chất tan, đơn vị là gam (g); mdd là khối lượng dung dịch, đơn vị là gam (g).
- Nồng độ mol:
Nồng độ mol (CM) của một dung dịch cho biết số mol chất tan có trong 1 lít dung dịch. Nồng độ mol được xác định bằng công thức:
CM = n / V
Trong đó: CM là nồng độ mol của dung dịch, có đơn vị là mol/l và thường được biểu diễn là M; n là số mol chất tan, đơn vị là mol; V là thể tích dung dịch, đơn vị là lít (L).
III. Trắc nghiệm Khoa học tự nhiên 8 Kết nối tri thức Bài 4 (có đáp án)
Câu 1: Dung dịch chưa bão hòa là
A. Dung dịch có thể hòa tan thêm chất tan
B. Tỉ lệ 2:1 giữa chất tan và dung môi
C. Tỉ lệ 1:1 giữa chất tan và dung môi
D. Làm quỳ tím hóa đỏ
Giải thích:
Dung dịch chưa bão hòa là dung dịch có thể hòa tan thêm chất tan. Ví dụ: Khi cho đường nào nước, lúc đầu đường tan hoàn toàn. Tiếp tục cho thêm đường vào nước đến khi không thể hòa tan thêm đường nữa, khi đó ta được dung dịch bão hòa.
Câu 2: Hai chất không thể hòa tan với nhau tạo thành dung dịch là
A. Nước và đường
B. Dầu ăn và xăng
C. Rượu và nước
D. Dầu ăn và cát
Giải thích:
- Dầu ăn là chất lỏng
- Cát là chất rắn
=> Không thể hòa tan
Câu 3: Khi hòa tan dầu ăn trong cốc xăng thì xăng đóng vai trò gì
A. Chất tan
B. Dung môi
C. Chất bão hòa
D. Chất chưa bão hòa
Câu 4: Nồng độ của dung dịch tăng nhanh nhất khi nào?
A. Tăng lượng chất tan đồng thời tăng lượng dung môi
B. Tăng lượng chất tan đồng thời giảm lượng dung môi
C. Tăng lượng chất tan đồng thời giữ nguyên lượng dung môi
D. Giảm lượng chất tan đồng thời giảm lượng dung môi
Câu 5: Độ tan của chất rắn phụ thuộc vào?
A. Nhiệt độ
B. Áp suất
C. Loại chất
D. Môi trường
Giải thích:
- Độ tan của chất rắn phụ thuộc vào nhiệt độ. Phần lớn tăng nhiệt độ thì độ tan của chất rắn tăng (trừ số ít trường hợp như Na2SO4…)
>>> Xem toàn bộ: Lý thuyết Khoa học tự nhiên 8 Kết nối tri thức
-------------------------------------------
Trên đây Toploigiai đã cùng các bạn Lý thuyết Khoa học tự nhiên 8 Kết nối tri thức Bài 4. Dung dịch và nồng độ theo chương trình Sách mới ngắn gọn nhất. Mời các bạn hãy click ngay vào trang chủ Toploigiai để tham khảo và chuẩn bị bài cho năm học mới Lớp 8 nhé. Chúc các bạn học tốt.
