Tóm tắt Lý thuyết Hóa 10 Kết nối tri thức Bài 10
Tóm tắt Lý thuyết Hóa học 10 Kết nối tri thức Bài 10: Quy tắc octet theo chương trình Sách mới ngắn gọn nhất. Tổng hợp lý thuyết Hóa học 10 trọn bộ chi tiết, đầy đủ.
Bài 10: Quy tắc octet
I. Khái niệm liên kết hóa học
- Liên kết hóa học là sự kết hợp giữa các nguyên tử tạo thành phân tử hay tinh thể bền vững hơn
- Khi tạo thành liên kết hóa học thì nguyên tử có xu hướng đạt tới cấu hình electron bền vững của khí hiếm
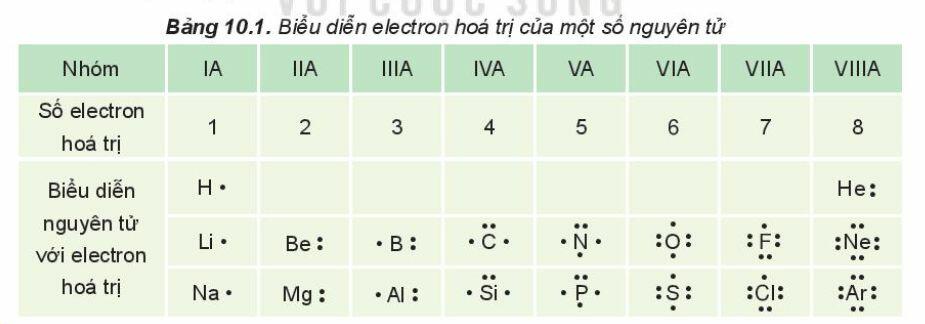
- Trong các phản ứng hóa học, chỉ có các electron thuộc lớp ngoài cùng và phân lớp sát lớp ngoài cùng tham gia vào quá trình tạo thành liên kết (electron hóa trị)
II. Quy tắc octet
Khi hình thành liên kết hóa học, các nguyên tử có xu hướng nhường, nhận hoặc góp chung electron để đạt tới cấu hình electron bền vững của nguyên tử khí hiếm. Vì các khí hiếm (trừ helium) đều có 8 electron lớp ngoài cùng nên quy tắc này được gọi là quy tắc octet.
Ví dụ 1: Xét sự hình thành liên kết hóa học trong phân tử Cl2.
- Cấu hình electron của nguyên tử Cl (Z = 17): [Ne]3s23p5.
- Khi hình thành liên kết hóa học trong phân tử Cl2, nguyên tử Cl có 7 electron hóa trị, mỗi nguyên tử Cl cần thêm 1 electron để đạt cấu hình electron bão hòa theo quy tắc octet nên mỗi nguyên tử Cl góp chung 1 electron.
- Phân tử Cl2 được biểu diễn:

- Xung quanh mỗi nguyên tử Cl đều có 8 electron.
Ví dụ 2: Vận dụng quy tắc octet trong sự tạo thành phân tử NaF.
- Nguyên tử sodium có 1 electron ở lớp ngoài cùng. Nếu mất đi 1 electron nguyên tử sodium sẽ tạo thành hạt mang điện dương, có cấu hình electron bền vững, giống với khí hiếm gần nhất là Ne.
Viết gọn: Na → Na+ + 1e
- Nguyên tử fluorine có 7 electron ở lớp ngoài cùng. Khi nhận vào 1 electron nguyên tử fluorine sẽ tạo thành hạt mang điện âm, có cấu hình electron bền vững giống khí hiếm Ne.
Viết gọn: F + 1e → F-
→ Các hạt tạo thành Na+; F- có điện tích trái dấu hút nhau tạo nên phân tử NaF.
>>> Xem toàn bộ:
- Lý thuyết Hóa 10 Kết nối tri thức
- Soạn Hóa 10 Kết nối tri thức
- Sơ đồ tư duy Hóa 10 Kết nối tri thức
- Trắc nghiệm Hóa 10 Kết nối tri thức
-------------------------------------------
Trên đây Toploigiai đã cùng các bạn Tóm tắt Lý thuyết Hóa học 10 Kết nối tri thức Bài 10: Quy tắc octet theo chương trình Sách mới ngắn gọn nhất. Mời các bạn hãy click ngay vào trang chủ Toploigiai để tham khảo và chuẩn bị bài cho năm học mới Lớp 10 nhé. Chúc các bạn học tốt.
