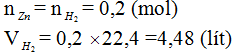Đề thi Học kì 2 Hóa 8 có đáp án - Đề 17
Đề thi Học kì 2 Hóa 8 có đáp án - Đề 17
ĐỀ BÀI
I.TRẮC NGHIỆM: (3 điểm)
Khoanh tròn chữ cái (A, B, C, D) đứng trước câu trả lời đúng
Câu 1. Phản ứng nào sau đây là phản ứng phân hủy?
A.CO2 + Ca(OH)2 ![]() CaCO3 + H2O B. CaO + H2O
CaCO3 + H2O B. CaO + H2O ![]() Ca(OH)2
Ca(OH)2
C. 2KMnO4 ![]() K2MnO4 + MnO2 + O2 D. CuO + H2
K2MnO4 + MnO2 + O2 D. CuO + H2![]() Cu + H2O
Cu + H2O
Câu 2. Dung dịch tạo thành khi cho nước hóa hợp với Na2O sẽ làm cho quỳ tím chuyển sang màu gì?
A. Màu đỏ B. Màu xanh C. Màu vàng D. Không đổi màu
Câu 3. Khử 12g sắt (III) oxit bằng khí hiđro ở nhiệt độ cao. Thể tích khí hiđro(ở đktc) cần dùng là:
A. 5,04 lít B. 7,56 lít C. 10,08 lít D. 8,2 lít
Câu 4. Dãy nào sau đây gồm các chất đều thuộc loại axit?
A. H3PO4, S, NaOH B. H3PO4, CuO, Na2CO3
C. HNO3, K, KCl D. HCl, H2S, H2SO4
Câu 5. Khối lượng NaOH có trong 20 gam dung dịch NaOH 10% là:
A. 20 (g) B. 2 (g) C. 0,2 (g) D. 0,02 (g)
Câu 6. Để tổng hợp nước người ta đã đốt cháy hoàn toàn 4,48 lít khí hiđro (đktc) trong oxi. Thể tích khí oxi (đktc) cần dùng là:
A. 44,8 lít B. 4,48 lít C. 2,24 lít D. 22,4 lít
Câu 7. Trộn 5 ml rượu etylic (cồn) với 10 ml nước cất. Câu nào sau đây diễn đạt đúng:
- Chất tan là rượu, dung môi là nước.
- Chất tan là nước, dung môi là rượu.
- Nước hoặc rượu etylic có thể là chất tan hoặclà dung môi.
- Cả 2 chất nước và rượu etylic vừa là chất tan vừa là dung môi.
Câu 8. Khi giảm nhiệt độ và tăng áp suất thì độ tan của chất khí trong nước thay đổi như thế nào?
A.Giảm B. Không thay đổi C. Có thể tăng hoặc giảm D. Tăng
Câu 9. Dung dịch NaCl 1M có nghĩa là:
- Trong 100 gam dung dịch có 1 gam NaCl.
- Trong 100 gam dung dịch có 1 mol NaCl.
- Trong 1 lít dung dịch có 1 mol NaCl.
- Trong 1000 ml dung dịch có 10 mol NaCl.
Câu 10. Dung dịch là hỗn hợp:
- Của chất rắn trong chất lỏng.
- Của chất khí trong chất lỏng.
- Đồng nhất của chất rắn và dung môi.
- Đồng nhất của dung môi và chất tan.
Câu 11. Có thể thu khí hidro bằng phương pháp đẩy nước và đẩy không khí vì hidro:
A. Là chất khí B. Nhẹ hơn không khí và ít tan trong nước
C. Nặng hơn không khí D. Có nhiệt độ hóa lỏng thấp
Câu 12. Số mol Na2CO3 có trong 100 ml dung dịch 2M là:
A. 0,1 mol B. 0,15 mol C. 0,25 mol D. 0,2 mol
II. TỰ LUẬN: (7 điểm)
Bài 1. (1 điểm) Trình bày tính chất hóa học của nước và viết các phương trình hóa học minh họa.
Bài 2. (2 điểm) Hoàn thành dãy chuyển hóa sau (ghi rõ điều kiện phản ứng):
![]()
Bài 3. (1 điểm) Đọc tên các hợp chất sau:
a,PbO b. NaHCO3 c. Fe(OH)2 d. HNO3
Bài 4. (3 điểm) Khi cho 0,2 mol kẽm tác dụng với dung dịch có chứa 49 gam axit sunfuric.
- Viết phương trình phản ứng?
- Sau phản ứng chất nào còn dư?
- Tính thể tích khí hiđro thu được (ở đktc)?
( Biết: S = 32 ; O = 16; H = 1; Zn = 65; Fe=56 )
ĐÁP ÁN VÀ BIỂU ĐIỂM
I. TRẮC NGHIỆM: (3 điểm)
Đáp án đúng 0.25 đ/câu
|
Câu |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
|
Đáp án |
C |
B |
A |
D |
B |
C |
A |
D |
C |
C |
B |
D |
II. TỰ LUẬN: (7 điểm)
|
Câu |
Đáp án |
Biểu điểm |
|
Câu 1 (1 điểm) |
- Nêu được 3 tính chất hóa học của nước - Tác dụng với kim loại: 2Na + H2O → 2NaOH + H2 ↑ - Tác dụng với oxit bazơ: BaO + H2O → Ba(OH)2 - Tác dụng với oxit axit: SO3 + H2O → H2SO4 |
0.25 0.25
0.25
0.25 |
|
Câu 2 (2 điểm) |
2KClO3 3Fe + 2O2 Fe3O4 + 4H2 Fe + H2SO4 →FeSO4 + H2 ↑ Lưu ý: - Viết sai công thức không ghi điểm - Chưa cân bằng hoặc thiếu điều kiện: - 0,25đ/pthh |
0.5 0.5
0.5 0.5 |
|
Câu 3 (1 điểm) |
a. PbO: Chì oxit b. NaHCO3: Natri hiđrocacbonat c. Fe(OH)2: Sắt (II) hiđroxit d. HNO3: Axit nitric |
0.25 0.25 0.25 0.25 |
|
Câu 4 (3 điểm) |
a. Phương trình phản ứng: Zn + H2SO4 → ZnSO4 + H2 1 mol 1 mol 1 mol 1 mol Đề bài: 0,2 mol 0,5 mol 0,2 mol b. Dựa theo PTHH trên ta có tỉ lệ: c. Tính thể tích khí hiđro thu được theo số mol kim loại kẽm:
Lưu ý: - HS làm cách khác đúng vẫn tính điểm. |
0.5
0.5
0.5
0.5
0.5 0.5
|