Tính chất hóa học của muối Sunfat kèm trắc nghiệm có đáp án
Muối sunfat là một loại muối của Axit sunfuric. Các muối sunfat tồn tại rộng rãi trong tự nhiên. Đa số các loại muối sunfat đều được điều chế trực tiếp từ Axit sunfuric (H2SO4). Để hiểu rõ hơn về tính chất của muối sunfat, Toploigiai mời các bạn đọc bài viết Tính chất hóa học của muối Sunfat kèm trắc nghiệm có đáp án sau đây.
1. Định nghĩa muối sunfat
Ion sunfat là một ion có công thức hóa học là: SO4(2-). Khi các gốc này kết hợp với các ion kim loại sẽ tạo thành muối sunfat. Các muối sunfat tồn tại rộng rãi trong tự nhiên. Đa số các loại muối sunfat đều được điều chế trực tiếp từ Axit sunfuric (H2SO4).
>>> Tham khảo: Nêu cách nhận biết H2SO4 và muối sunfat?
2. Phân loại muối sunfat và cách nhận biết, tính chất hóa học của muối sunfat
Muối sunfat là một loại muối của Axit sunfuric, hiện nay có 2 loại muối sunfat:
Muối trung hòa (muối sunfat): Là muối chứa các ion sunfat SO4(2-). Đa số các loại muối Sunfat đều tan trong nước, trừ một số loại muối của Ba, Pb, Sr là không tan.
Muối axit (muối hidrosunfat): Là muối chứa các ion hidrosunfat (HSO4).
Để nhận biết dung dịch muối sunfat, ta dùng thuốc thử là dung dịch muối như BaCl2, Ba(NO3)2… hoặc dùng Ba(OH)2. Phản ứng tạo thành kết tủa trắng BaSO4 không tan trong nước và trong axit.
Ví dụ:
Phương trình hóa học: H2SO4 + BaCl2 → BaSO4↓ + 2HCl
Phương trình hóa học: Na2SO4+ BaCl2 → BaSO4 ↓ + 2NaCl
3.Tính chất hóa học Axit sunfuric
a. Tính chất vật lý
- Axit sunfuric là chất lỏng sánh như dầu, không màu, không bay hơi, nặng gấp 2 lần nước.
- Tan vô hạn trong nước và tỏa rất nhiều nhiệt.
Lưu ý: để pha loãng dung dịch H2SO4 đặc, ta cần rót từ từ axit vào nước, khuấy nhẹ và không làm ngược lại.
b. Tính chất hoá học
Ở trạng thái loãng là một axit mạnh, ở trạng thái đặc là một chất ôxi hóa mạnh.
- H2SO4 loãng mang những tính chất chung của một axit:
Làm đỏ quì tím, tác dụng kim loại (trước H) giải phóng H2, tác dụng bazơ, oxit bazơ và nhiều muối.
H2SO4 + Fe → FeSO4 + H2
H2SO4 + 2NaOH → Na2SO4 + 2H2O
H2SO4 + CuO → CuSO4 + H2O
- Ở dạng đặc là một chất oxi hóa mạnh
+ Tác dụng với kim loại: oxi hoá hầu hết các kim loại (trừ Au và Pt) tạo muối hoá trị cao và thường giải phóng SO2 (có thể H2 S, S nếu kim loại khử mạnh như Mg ).
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2 + 6H2O
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
Al, Fe, Cr không tác dụng với H2SO4 đặc nguội, vì kim loại bị thụ động hóa.
+ Tác dụng với phi kim ( tác dụng với các phi kim ở dạng rắn, to) tạo hợp chất của phim kim ứng với số oxi hóa cao nhất.
C + 2H2SO4 → CO2 + 2SO2 + 2H2O
S + 2H2SO4 → 3SO2 + 2H2O
+ Tác dụng với một số chất có tính khử
FeO + H2SO4 → Fe2(SO4)3 + SO2 + 4H2O
HBr + H2SO4 → Br2 + SO2 + 2H2O
+ Hút nước của 1 số chất hữu cơ:
C12H22O11 + H2SO4(đ) → 12C + H2SO4 .11H2O
c. Ứng dụng
- Axit sunfuric là hoá chất hàng đầu được dùng trong nhiều ngành sản xuất. Hàng năm, các nước trên thế giới sản xuất khoảng 160 triệu tấn H2SO4.
- Axit sunfuric được dùng để sản xuất phân bón, thuốc trừ sâu, chất giặt rửa tổng hợp, tơ sợi hoá học, chất dẻo, sơn màu, phẩm nhuộm, dược phẩm, chế biến dầu mỏ...
d. Sản xuất axit sunfuric
Axit sunfuric được sản xuất trong công nghiệp bằng phương pháp tiếp xúc bao gồm 3 công đoạn chính:
* Sản xuất lưu huỳnh đioxit (SO2)
Đốt cháy lưu huỳnh hoặc quặng pirit sắt FeS2
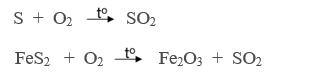
* Sản xuất lưu huỳnh trioxit (SO3)
Oxi hóa SO2 bằng khí oxi hoặc không khí dư ở nhiệt độ khoảng từ 450oC - 500oC với chất xúc tác là vandi (V) oxit V2O5:
* Hấp thụ SO3 bằng H2SO4
Dùng H2SO4 98% hấp thụ SO3, thu được oleum H2SO4.nSO3:
H2SO4 + nSO3 → H2SO4.nSO3
Sau đó dùng lượng nước thích hợp pha loãng oleum sẽ thu được H2SO4 đặc:
H2SO4.nSO3 + nH2O → (n+1)H2SO4
>>> Tham khảo: Hãy nêu cách nhận biết axit sunfuric và muối sunfat?
4. Bài tập trắc nghiệm có đáp án
Câu 1: Các pha loãng H2SO4 đặc an toàn là:
A. Rót nhanh axit vào nước và khuấy đều
B. Rót nhanh nước vào axit và khuấy đều
C. Rót từ từ nước vào axit và khuấy đều
D. Rót từ từ axit vào nước và khuấy đều
Đáp án: D
Câu 2: Khi lần lượt tác dụng với mỗi chất dưới đây, trường hợp nào axit sunfuric đặc và axit sunfuaric loãng hình thành sản phẩm giống nhau?
A. Mg
B. Fe3O4
C. CaCO3
D. Fe(OH)2
Đáp án: C
Câu 3: Dãy kim loại nào trong các dãy sau đây gồm các kim loại đều không tác dụng với dung dịch H2SO4 loãng?
A. Al, Mg, Cu
B. Fe, Mg, Ag
C. Al, Fe, Mg
D. Al, Fe, Cu
Đáp án: C
Câu 4: Trong số những tính chất sau, tính chất nào không là tính chất của axit sunfuaric đặc nguội?
A. Làm hóa than vải, giấy, đường saccarozo
B. Tan trong nước, tỏa nhiệt
C. Háo nước
D. Hòa tan được kim loại Fe, Al
Đáp án: D
Câu 5: Axit H2SO4 đặc có thể làm khô khí nào sau đây là tốt nhất?
A. H2S
B. SO3
C. CO2
D. CO
Đáp án: C
Câu 6: Những người bị bệnh đau dạ dày thường cần uống loại hóa chất nào sau đây?
A. NaHSO3
B. Na2CO3
C. Na2SO3
D. NaHCO3
Đáp án: D
Câu 7: Cho phương trình hóa học: aAl + bH2SO4 → cAl2(SO4)3+ dSO2 + eH2O. Tỉ lệ a:b là?
A. 1:1
B. 2:3
C. 1:3
D. 1:2
Đáp án: C
Câu 8: Hòa tan hoàn toàn 3,22 gam hỗn hợp X gồm Fe, Mg và Zn bằng 1 lượng vừa đủ dung dịch H2SO4 loãng, thu được 1,344 lít khí hidro (đktc) và dung dịch chứa m gam muối. Giá trị của m là
A. 9,52
B. 10,27
C. 8,98
D. 7,25
Đáp án: C
Câu 9: Phương trình hóa học nào sau đây không đúng?
A. Cu + 2H2SO4(đặc) → CuSO4 +SO2 + 2H2O
B. Fe + S → FeS
C. 2Ag + O3 → Ag2O + O2
D. 2Fe + 3H2SO4(loãng) → Fe2(SO4)3 + 3H2
Đáp án: D
Câu 10: Hòa tan hết 0,2 mol FeO bằng dung dịch H2SO4 đặc, nóng (dư), thu được khí SO2 (sản phẩm khử duy nhất). Hấp thụ hoàn toàn khí SO2 sinh ra ở trên vào dung dịch chứa 0,13 mol KOH, thu được dung dịch chứa m gam muối. Giá trị của m là
A. 15,80
B. 14,66
C. 15,60
D. 13,14
Đáp án: D
--------------------------------
Như vậy, Toploigiai đã tổng hợp kiến thức về Tính chất hóa học của muối sunfat kèm trắc nghiệm có đáp án, đồng thời bổ sung thêm kiến thức về axit sunfuric. Hi vọng các bạn có những kiến thức bổ ích khi đọc bài viết này, chúc các bạn học tập tốt.
