Bài 6 trang 155 SGK Hóa 9
Mục lục nội dung
Bài 51: Saccarozơ
Bài 6 (trang 155 SGK Hóa 9)
Khi đốt cháy một loại gluxit (thuộc một trong các chất sau: Glucozơ, saccarozơ), người ta thu được khối lượng H2O và CO2 theo tỉ lệ 33: 88. Xác định công thức của gluxit trên.
Lời giải:
Qua công thức glucozơ: C6H12O6 và saccarozơ C12H22O11 ta nhận thấy nH=2nO
Nên ta đặt công thức của gluxit có dạng là CnH2mOm.
Phản ứng đốt cháy:
CnH2mOm + nO2 → nCO2↑ + mH2O.
Theo đề bài ta có tỉ lệ khối lượng giữa H2O và CO2 là 33:88
Giả sử số mol của gluxit là 1(mol)
⇒ nCO2 = n mol⇒ mCO2 = n × M = n × 44(g)
nH2O= m mol ⇒ mH2O = m × M = m × 18(g)
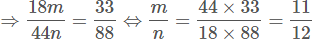
Công thức phù hợp là C12H22O11.
Xem toàn bộ Giải Hóa 9: Bài 51. Saccarozơ
Xuất bản : 04/02/2021 - Cập nhật :
27/07/2021
Câu hỏi thường gặp
Tìm Kiếm Bài Viết
