Lý thuyết Vật lý 11 Bài 14. Dòng diện trong chất điện phân
Lý thuyết Vật lý 11 Bài 14. Dòng điện trong chất điện phân
I. Thuyết điện li
Trong dung dịch, các hợp chất hoá học như axit, bazơ và muối bị phân li (một phần hoặc toàn bộ) thành các nguyên tử (hoặc nhóm nguyên tử) tích điện gọi là ion; ion có thể chuyển động tự do trong dung dịch và trở thành hạt tải điện.
Ta gọi chung những dung dịch và chất nóng chảy (muối hoặc bazơ nóng chảy) là chất điện phân.
II. Bản chất dòng điện trong chất điện phân
Dòng điện trong lòng chất điện phân là dòng ion dương và ion âm chuyển động có hướng theo hai chiều ngược nhau.
Chất điện phân không dẫn điện tốt bằng kim loại.
Dòng điện trong chất điện phân không chỉ tải điện lượng mà còn tải cả vật chất (theo nghĩa hẹp) đi theo. Tới điện cực chỉ có êlectron có thể đi tiếp, còn lượng vật chất đọng lại ở điện cực, gây ra hiện tượng điện phân.
III. Các hiện tượng diễn ra ở điện cực. Hiện tượng dương cực tan
Hiện tượng dương cực tan xảy ra khi các anion đi tới anôt kéo các ion kim loại của điện cực vào trong dung dịch.
IV. Các định luật Fa-ra-đây
1. Định luật Fa-ra-đây thứ nhất
Khối lượng vật chất được giải phóng ở điện cực của bình giải phóng ở điện điện phân tỉ lệ thuận với điện lượng chạy qua bình đó.
m = kq
2. Định luật Fa-ra-đây thứ hai
Đương lượng điện hoá k của một nguyên tố tỉ lệ với đương lượng gam
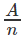
của nguyên tố đó. Hệ số tỉ lệ là
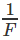
, trong đó F gọi là số Fa-ra-đây.
F = 96 494 C/mol ≈ 96 500 C/mol.
Kết hợp hai định luật Fa-ra-đây, ta được công thức Fa-ra-đây:
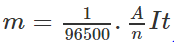
m là khối lượng của chất được giải phóng ở điện cực, tính bằng gam, A là khối lượng mol nguyên tử của chất, I tính bằng ampe, t tính bằng giây, n là hoá trị của nguyên tố tạo ra ion.
V. Ứng dụng của hiện tượng điện phân
Hiện tượng điện phân được áp dụng trong các công nghệ luyện kim, hoá chất, mạ điện.
Xem thêm Giải bài tập Vật lý 11: Bài 14. Dòng điện trong chất điện phân
