Lý thuyết Hóa 10 Bài 23. Hiđro clorua, axit clohiđric và muối clorua
Lý thuyết Hóa 10 Bài 23. Hiđro clorua, axit clohiđric và muối clorua
I. HIĐRO CLORUA
1. Cấu tạo phân tử
Hiđro clorua là hợp chất cộng hóa trị, phân tử có cực:
![]()
(Hiệu độ âm điện giữa nguyên tử clo và nguyên tử hiđro là 3,16 – 2,2 0= 0,96
2. Tính chất
- Hiđro clorua là chất khí không màu, mùi xốc, độc.
![]()
⟹ Nặng hơn không khí.
- Khí HCl tan rất nhiều trong nước tạo thành dung dịch axit HCl (ở 20oC, 1 lít nước hòa tan gần 500 lít khí HCl).
II. AXIT CLOHIĐRIC
1. Tính chất vật lí
- Chất lỏng không màu, mùi xốc.
- Khối lượng riêng D=1,19 g/cm3.
- Dung dịch HCl đậm đặc bốc khói trong không khí ẩm.
2. Tính chất hóa học
a) Tính axit: Axit HCl là axit mạnh
* Làm quỳ tím (xanh) ⟶ đỏ.
* Tác dụng với kim loại (Đứng trước H)
![]()
(n là hóa trị thấp nhất của kim loại M)
Ví dụ:
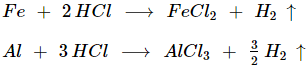
* Tác dụng với oxit bazơ, bazơ
![]()
Ví dụ:
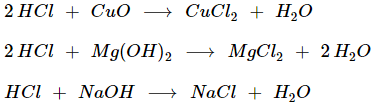
* Tác dụng với muối
HCl + Muối ⟶ Muối clorua + Axit (mới)
(Sản phẩm phải có muối clorua ↓ hay axit (mới) là axit yếu, dễ bay hơi)
Ví dụ:
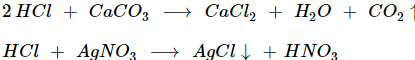
b) Tính khử: Do trong phân tử HCl, nguyên tố clo có số oxi hóa thấp nhất là −1
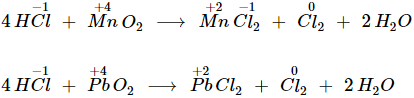
3. Điều chế
a) Trong phòng thí nghiệm
Cho tinh thể NaCl tác dụng với axit H2SO4 đậm đặc và đun nóng (phương pháp sunfat):
![]()
Ở nhiệt độ cao hơn:
![]()
Khí HCl hòa tan vào nước ⟶ dung dịch axit HCl.
b) Trong công nghiệp
- Tổng hợp từ H2 và Cl2C:
![]()
- Phương pháp sunfat (với to ≥ 400oC) cũng được áp dụng trong công nghiệp.
- Thu HCl từ phản ứng clo hóa các hợp chất hữu cơ:
CH4 + Cl2 ⟶ CH3Cl + HCl
III. MUỐI CLORUA VÀ NHẬN BIẾT ION CLORUA
1. Một số muối clorua
- Muối của axit clohiđric gọi là muối clorua.
- Đa số muối clorua tan nhiều trong nước, trừ một số muối clorua không tan trong nước như AgCl↓(trắng) và ít tan như PbCl2↓(trắng), CuCl↓(trắng)...
* Ứng dụng:
- NaCl: dùng làm muối ăn, điều chế NaOH, Cl2, H2, nước Gia-ven, axit HCl...
- KCl: dùng làm phân kali.
- ZnCl2: có khả năng diệt khuẩn, làm chất chống mục gỗ.
- AlCl3: chất xúc tác trong tổng hợp hữu cơ.
- BaCl2: trừ sâu bệnh trong nông nghiệp.
2. Nhận biết ion clorua
- Thuốc thử: dung dịch AgNO3.
- Dấu hiệu phân biệt: Khi nhỏ dung dịch AgNO3 vào dung dịch axit HCl hay dung dịch muối clorua tạo kết tủa trắng (AgCl)
NaCl+AgNO3⟶AgCl↓+NaNO3
HCl+AgNO3⟶AgCl↓+HNO3
Xem thêm Giải Hóa 10: Bài 23. Hiđro clorua - Axit clohiđric và muối clorua
