Lý thuyết Hóa 9 Bài 29. Axit cacbonic và muối cacbonat
Lý thuyết Hóa 9 Bài 29. Axit cacbonic và muối cacbonat
I. AXIT CACBONIC H2CO3
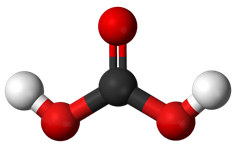
a) Trạng thái tự nhiên và tính chất vật lí
Nước tự nhiên và nước mưa có hòa tan khí cacbonic: 1000m3 nước hòa tan được 90 m3 khí CO2.
Một phần khí CO2 tác dụng với nước tạo thành dung dịch axit cacbonic. Vậy axit R2CO3 có trong nước tự nhiên và nước mưa. Khi đun nóng, khí CO2 bay ra khỏi dung dịch.
b) Tính chất hóa học
– H2CO3 là một axit yếu, dung dịch H2CO3 chỉ làm quỳ tím chuyển thành màu đỏ nhạt, bị axit mạnh đẩy ra khỏi muối.
– H2CO3 là một axit không bền: H2CO3 tạo thành trong các phản ứng hóa học bị phân hủy ngay thành CO2 và H2O.
II. MUỐI CACBONAT
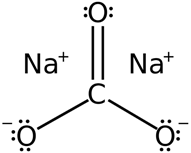
a) Phân loại: Có 2 loại là muối trung hòa (Na2CO3, CaCO3,..) và muối axit (NaHCO3, Ca (HCO3)2…).
b) Tính chất
– Tinh tan
– Chỉ có một số muối cacbonat tan dược, như Na2CO3, K2CO3… và muối axit như Ca (HCO3)2,…
– Hầu hết muối cacbonat trung hòa không tan, như CaCOg, BaCOg, MgCO3r..
c) Tính chất hóa học
– Tác dụng với axit mạnh (HCl, HNO3, H2SO4,…) giải phóng khí CO2.
NaHCO3 + HCl → NaCl + CO2 + H2O
– Muối cacbonat tan tác dụng được với dung dịch bazơ.
K2CO3 + Ca(OH)2 → 2KOH + CaCO3
– Muối cacbonat tan tác dụng được với dung dịch muối.
Na2CO3 + CaCl2 → 2NaCl + CaCO3
– Bị nhiệt phân hủy.
![]()
Chú ý: Các muối Na2CO3, K2CO3,… không bị nhiệt phân.
III. ỨNG DỤNG
– CaCO3 là thành phần chính của đá vôi, được dùng để sản xuất vôi, xi măng..
– Na2CO3 được dùng để nấu xà phòng, sản xuất thủy tinh,..
– NaHCO3 được dùng làm dược phẩm, hóa chất trong bình cứu hỏa,
