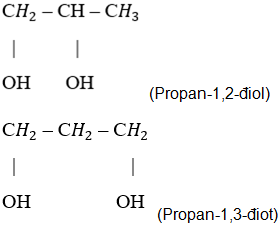
Bài 42. Luyện tập: Dẫn xuất halogen, ancol, phenol
Bài 42. Luyện tập: Dẫn xuất halogen, ancol, phenol
Bài 42.1 trang 66 SBT Hóa 11:
Có bao nhiêu chất đồng phân có cùng công thức phân C4H10O
A. 7 chất
B. 6 chất
C. 5 chất
D. 4 chất
Lời giải:
Đáp án: A. Trong 7 đồng phân C4H10O có 4 ancol và 3 ete.
Bài 42.2 trang 66 SBT Hóa 11:
Có bao nhiêu ancol bậc I có cùng công thức phân tử C5H10O?
A. 6 chất
B. 5 chất
C. 4 chất
D. 3 chất
Lời giải:
Đáp án: C. Các ancol bậc I C5H10O phải có dạng C4H9CH2OH. Có 4 gốc -C4H9, vì vậy có 4 ancol C4H9CH2OH.
Bài 42.3 trang 66 SBT Hóa 11:
Cho lần lượt các chất C2H5Cl, C2H5OH, C6H5OH vào dung dịch NaOH đun nóng. Số chất phản ứng là ?
A. Không chất nào.
B. Một chất.
C. Hai chất.
D. Cả ba chất.
Lời giải:
Đáp án: C.
Bài 42.4 trang 67 SBT Hóa 11:
Đun chất sau với dung dịch NaOH có dư. Sản phẩm hữu cơ thu được là chất nào dưới đây ?
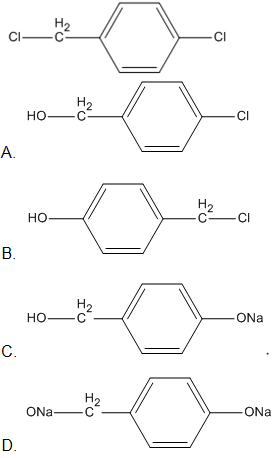
Lời giải:
Đáp án: A.
Bài 42.5 trang 67 SBT Hóa 11:
Trong các phương trình hóa học dưới đây, phương trình nào sai?
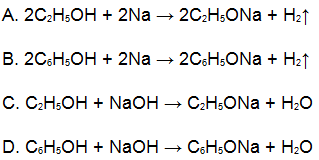
Lời giải:
Đáp án: C.
Bài 42.6 trang 67 SBT Hóa 11:
Ancol X có công thức phân tử C4H10O. Khi đun X với H2SO4 đặc ở 170oC, thu được hai anken là đồng phân của nhau. Công thức cấu tạo của X là
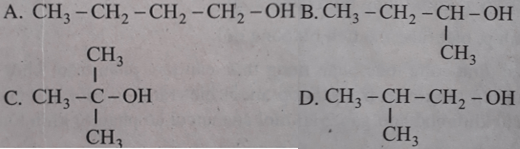
Lời giải:
Đáp án: B.
Bài 42.7 trang 67 SBT Hóa 11:
Viết phương trình phản ứng hóa học thực hiện các biến hóa dưới đây. Ghi rõ điều kiện của phản ứng (nếu có).
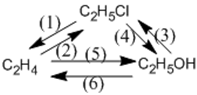
Lời giải:
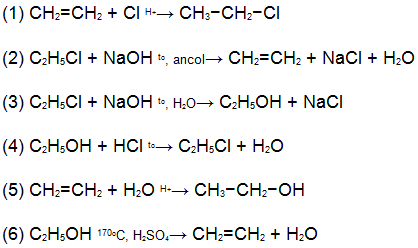
Bài 42.8 trang 67 SBT Hóa 11:
Cho chất sau lần lượt tác dụng với
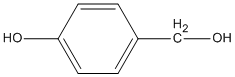
1. Na;
2. dung dịch NaOH;
3. dung dịch HBr;
4. CuO (đun nóng nhẹ).
Viết phương trình hoá học của các phản ứng xảy ra.
Lời giải:
1. HO−C6H4−CH2OH + 2Na → Na−O−C6H4−CH2−ONa + H2
2. HO−C6H4−CH2OH + NaOH → NaO−C6H4−CH2OH + H2O
3. HO−C6H4−CH2OH + HBr → HO−C6H4−CH2Br + H2O
4. HO−C6H4−CH2OH + CuO → HO−C6H4−CHO + Cu + H2O
Bài 42.9 trang 67 SBT Hóa 11:
Chất A là một ancol no, đơn chức, mạch hở. Đun m gam A với H2SO4 đặc ở 170oC thu được 17,85 gam anken (hiệu suất 85%). Cũng m gam A khi tác dụng với HBr tạo ra 36,9 gam dẫn xuất brom (hiệu suất 60%).
1. Xác định công thức phân tử, công thức cấu tạo và tên của ancol A.
2. Tính giá trị m.
Lời giải:
1. Nếu hiệu suất các phản ứng là 100% thì:
- Khối lượng anken thu được là: ![]()
- Khối lương dẫn xuất brom thu đươc là: ![]()
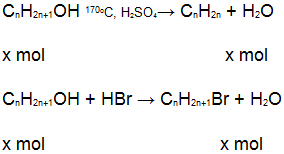
14nx = 21; (14n + 81)x = 61,5
⇒ x = 0,5; n = 3.
Ancol A có CTPT C3H8O và có CTCT
CH3 - CH2 - CH2 - OH ( propan-1-ol ) hoặc
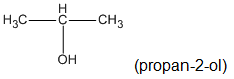
m = 0,5.60 = 30 (g)
Bài 42.10 trang 68 SBT Hóa 11:
Chất A là một ancol có mạch cacbon không phân nhánh. Đốt cháy hoàn toàn m gam A, người ta thu được 2,24 lít CO2 (đktc) và 2,25 g H2O. Mặt khác, nếu cho 18,55 g A tác dụng hết với natri, thu được 5,88 lít H2 (đktc).
1. Hãy xác định công thức phân tử, công thức cấu tạo và tên của chất A.
2. Tính giá trị m.
Lời giải:
1. Số mol CO2 ![]()
Số mol H2O ![]()
Khi đốt ancol A, số mol H2O tạo thành < số mol CO2. Vậy A phải là ancol no, mạch hở. A có dạng CnH2n+2-x(OH)x hay CnH2n+2Ox.
![]()
Theo đầu bài ta có:
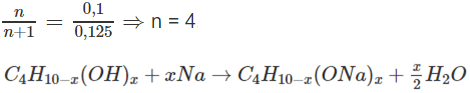
Theo phương trình : Cứ (58 + 16x) g A tạo ra 0,5000x mol H2.
Theo đầu bài:
Cứ 18,55 g A tạo ra ![]() mol H2.
mol H2.
![]()
CTPT của A là C4H10O3.
Theo đầu bài A có mạch cacbon không nhánh; như vậy các CTCT thích hợp là
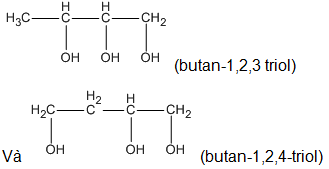
2. Để tạo ra 0,1 mol CO2;
Số mol A cần đốt là: ![]()
Như vậy: m = 0,025 x 106 = 2,65 (g).
Bài 42.11 trang 68 SBT Hóa 11:
Một bình kín dung tích 5,6 lít có chứa hỗn hợp hơi của hai ancol đơn chức và 3,2 g O2. Nhiệt độ trong bình là 109,2oC, áp suất trong bình là 0,728 atm.
Bật tia lửa điện để đốt cháy hoàn toàn hai ancol, sau phản ứng nhiệt độ trong bình là 136,5oC và áp suất là p atm.
Dẫn các chất trong bình sau phản ứng qua bình (1) đựng H2SO4 đặc (dư), sau đó qua bình (2) đựng dung dịch NaOH (dư), thấy khối lượng bình (1) tăng 1,26 g, khối lượng bình (2) tăng 2,2 g.
1. Tính p, biết rằng thể tích bình không đổi.
2. Xác định công thức phân tử, công thức cấu tạo, phần trăm khối lượng và gọi tên từng chất trong hỗn hợp ancol biết rằng số mol của ancol có phân tử khối nhỏ hn gấp 2 lần số mol của ancol có phân tử khối lớn hơn.
Lời giải:
1. Đổi thể tích hỗn hợp khí trong bình trước phản ứng về đktc:
![]()
Số mol các chất trong bình trước phản ứng là: ![]()
Số mol O2 = 0,1 (mol) ⇒ Số mol 2 ancol = 0,13 - 0,1 = 0,03 (mol).
Khi 2 ancol cháy :
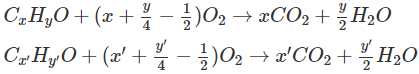
H2SO4 + nH2O → H2SO4.nH2O
2NaOH + CO2 → Na2CO3 + H2O
Số mol H2O là: ![]()
Số mol CO2 là: ![]()
Theo định luật bảo toàn khối lượng :
![]()
= 3,2 + 0,03.16 - 0,07.16 - 0,05.32 = 0,96 (g).
Số mol O2 còn dư: ![]()
Tổng số mol các chất trong bình sau phản ứng :
0,07 + 0,05 + 0,03 = 0,15 (mol).
Thể tích của 0,15 mol khí ở đktc là: V0 = 0,15.22,4 = 3,36 (lít).
Thực tế, sau phản ứng V = 5,6 lít.
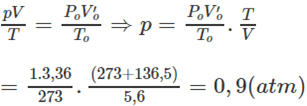
Giả sử CxHyO có PTK nhỏ hơn Cx'Hy'O; như vậy số mol CxHyO sẽ là O2và số mol Cx'Hy'O là 0,01.
Số mol CO2 sẽ là 0,02x + 0,01x' = 0,05 (mol) hay 2x + x' = 5.
x và x' là số nguyên: x = 1 ; x' = 3
hoặc x = 2; x' = 1
Cặp x = 2; x' = 1 loại vì trái với điều kiện: CxHyO có PTK nhỏ hơn Cx'Hy'O
Vậy, một ancol là CH4O và chất còn lại C3Hy′O.
Số mol H2O là 0,02.2 + 0,01.(y′/2) = 0,07 (mol).
⇒ y' = 6 ⇒ Ancol còn lại là C3H6O.
% về khối lượng của CH4O hay CH3 - OH (ancol metylic) :
![]()
% về khối lượng của C3H6O hay CH2 = CH - CH2 - OH (ancol anlylic): 100,00% - 52,46% = 47,54%.
Bài 42.12 trang 68 SBT Hóa 11:
Chất A là một ancol no mạch hở. Đốt cháy hoàn toàn 9,50 g chất A, thu được 8,40 lít CO2. Mặt khác nếu cho 11,40 g chất A tác dụng với Na (lấy dư) thì thu được 3,36 lít H2. Các thể tích đo ở đktc. Xác định công thức phân tử, công thức cấu tạo và tên chất A.
Lời giải:
Chất A là CnH2n+2-x(OH)x hay CnH2n+2Ox
Theo phương trình: ![]()
Cứ (14n + 16x + 2) g A tạo ra n mol CO2
Theo đầu bài:
Cứ 9,5g A tạo ra ![]() mol CO2
mol CO2
Vậy 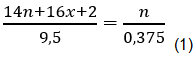
![]()
Theo phương trình:
Cứ (14n + 16x + 2)g A tạo ra ![]() mol H2
mol H2
Theo đầu bài:
Cứ 11,40g A tạo ra ![]() mol H2
mol H2
Vậy ![]() (2)
(2)
Giải hệ phương trình (1) và (2) tìm được x = 2; n = 3.
Công thức phân tử chất A: C3H8O2.
Công thức cấu tạo chất A: