Bài 31. Luyện tập. Anken và ankađien
Bài 31. Luyện tập: Anken và ankađien
Bài 31.1 trang 47 SBT Hóa 11:
Ghép tên chất với công thức cấu tạo cho đúng.
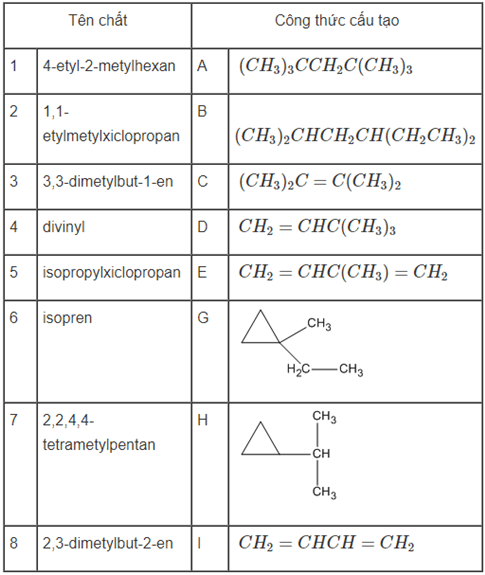
Lời giải:
Đáp số: 7-A; 1-B; 8-C; 3-D; 6-E; 2-G; 5-H; 4-I
Bài 31.2 trang 48 SBT Hóa 11:
Hợp chất sau có tên là gì?
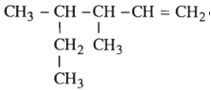
A. 2-etyl-3-metylpent-4-en.
B. 4-etyl-3-metylpen-1-en.
C. 3,4-đimetyl-hex-5-en.
D. 3,4-đimetyl-hex-1-en.
Lời giải:
Đáp án: D.
Bài 31.3 trang 48 SBT Hóa 11:
Hợp chất sau có tên là gì? 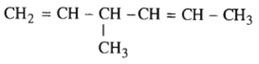
A. 3-metylhex-1,2-đien.
B. 4-metylhex-1,5-đien.
C. 3-metylhex-l,4-đien.
D. 3-metylhex-1,3-đien.
Lời giải:
Đáp án: C.
Bài 31.4 trang 48 SBT Hóa 11:
Trong các chất dưới đây, chất nào là ankađien liên hợp ?
A. CH2= CH - CH2- CH = CH2
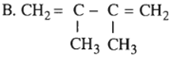
C. CH2= CH - CH2- CH = CH - CH3
D. CH2= C = CH2
Lời giải:
Đáp án: B.
Bài 31.5 trang 48 SBT Hóa 11:
Cho chất 2-metylbut-2-en phản ứng cộng với nước, sản phẩm chủ yếu thu được sẽ là
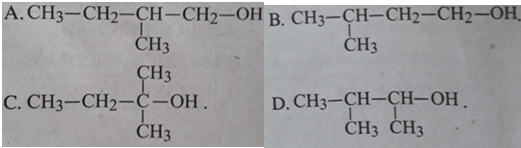
Lời giải:
Đáp án: C.
Bài 31.6 trang 49 SBT Hóa 11:
Cho đivinyl phản ứng cộng với HBr theo tỉ lệ 1 : 1 (về số mol) ở 40oC thì sản phẩm chính thu được là
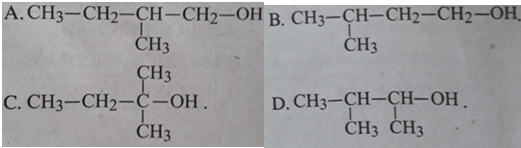
Lời giải:
Đáp án: C.
Bài 31.7 trang 49 SBT Hóa 11:
Hỗn hợp khí A chứa nitơ và hai hiđrocacbon kế tiếp nhau trong một dãy đồng đẳng. Khối lượng hỗn hợp A là 18,3 g và thể tích của nó là 11,2 lít. Trộn A với một lượng dư oxi rồi đốt cháy, thu được 11,7 gam H2O và 21,28 lít CO2. Các thể tích đo ở đktc.
Hãy xác định công thức phân tử và phần trăm về khối lượng của từng hiđrocacbon trong hỗn hợp A.
Lời giải:
Số mol CO2 ![]()
Khối lượng C trong A là: 0,95.12 = 11,4 (g).
Số mol H2O ![]()
Khối lượng H trong A là: 0,65.2 = 1,3 (g).
Tổng khối lượng của C và H chính là tổng khối lượng 2 hiđrocacbon. Vậy, khối lượng N2 trong hỗn hợp A là : 18,30 - (11,4 + 1,3) = 5,6 (g)
Số mol N2 ![]()
Số mol 2 hidrocacbon ![]()
Đặt lượng CxHy là a mol, lượng Cx+1Hy+2 là b mol :
a + b = 0,2 (1)
Số mol C = số mol CO2, do đó :
xa + (x + 1)b = 0,95 (2)
Số mol H = 2.số mol H2O, do đó :
ya + (y + 2)b = 2. 0,65= 1,3
Từ (2) ta có x(a + b) + b = 0,95 ⇒ b = 0,95 - 0,3x
Vì 0 < b < 0,3, nên 0 < 0,95 - 0,3x < 0,3
Từ đó tìm được 2,16 < x < 3,16 ⇒ x = 3.
⇒ b = 0,95 − 3.0,3 = 5.10−2
⇒ a = 0,3 − 0,05 = 0,25
Thay giá trị tìm được của a và b vào (3), ta có y = 4.
% về khối lượng của C3H4 trong hỗn hợp A:
![]()
% về khối lượng của C4H6 trong hỗn hợp A :
![]()