Bài 6 trang 129 SGK Hóa 12
Mục lục nội dung
Bài 27. Nhôm và hợp chất của nhôm
Bài 6 (trang 129 SGK Hóa 12)
Cho 100 ml dung dịch AlCl3 1M tác dụng với 200ml dung dịch NaOH. Kết tủa tạo thành được làm khô và nung đến khối lượng không đổi cân nặng 2,55g. Tính nồng độ dung dịch NaOH ban đầu.
Lời giải:
Số mol AlCl3 là nAlCl3 = 0,1. 1 = 0,1 (mol)
Số mol Al2O3 là:
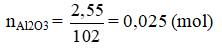
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl (1)
0,1(mol) 0,1(mol)
2Al(OH)3 + 2NaOH → 2NaAlO2 + 3H2O (2)
0,05(mol)
2 Al(OH)3 t0→ Al2O3 + 3H2O (3)
0,05(mol) 0,025(mol)
Theo pt (3) ta thấy nAl(OH)3 = 2. nAl2O3 = 2. 0,025 = 0,05 (mol)
Như vậy đã có: 0,1 - 0,05 = 0,05 (mol) Al(OH)3 đã bị hòa tan ở pt (2)
Từ (1) và (2) số mol NaOH = 3.0,1 + 0,05 = 0,35 (mol)
Nồng độ mol/l:
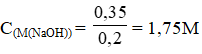
Xem toàn bộ Giải Hóa 12: Bài 27. Nhôm và hợp chất của nhôm
Xuất bản : 04/02/2021 - Cập nhật :
30/07/2021
Câu hỏi thường gặp
Tìm Kiếm Bài Viết
