Bài 4 trang 159 SGK Hóa 12
Mục lục nội dung
Bài 35. Đồng và hợp chất của đồng
Bài 4 (trang 159 SGK Hóa 12)
Đốt 12,8 gam Cu trong không khí, hòa tan chất rắn thu được trong dung dịch HNO3 0,5M thấy thoát ra 448ml khí NO duy nhất (đktc).
a) Viết phương trình phản ứng hóa học xảy ra.
b) Tính thể tích tối thiểu dung dịch HNO3 cần dùng để hòa tan chất rắn.
Lời giải:
a) 2Cu + O2 → 2CuO (1)
3CuO + 8HNO3 → 3Cu(NO3)2 + 2NO + H2O (2)
CuO + 2HNO3 → Cu(NO3)2 + 2H2O (3)
b)
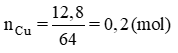
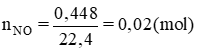
Gọi nCu phản ứng = x mol ⇒ nCu dư = 0,2 – x (mol)
Theo pt (3):
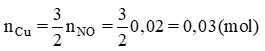
⇒ 0,2 – x = 0,03 ⇒ x = 0,17 mol
Theo pt: nCuO = nCu pư = x = 0,17 mol
nHNO3 = 2. nCuO + 4. nNO = 2. 0,17 + 4. 0,02 = 0,42 mol
Vậy thể tích dung dịch HNO3 cần dùng là:
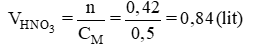
Xem toàn bộ Giải Hóa 12: Bài 35. Đồng và hợp chất của đồng
Xuất bản : 04/02/2021 - Cập nhật :
30/07/2021
Câu hỏi thường gặp
Tìm Kiếm Bài Viết
