Bài 6 trang 166 SGK Hóa 10 nâng cao
Bài 42: Ozon và hiđro peoxit
Bài 6 (trang 166 SGK Hóa 10 nâng cao)
Hỗn hợp khí A gồm có O2 và O3, tỉ khối của hỗn hợp khí A đối với hiđro là 19,2. Hỗn hợp khí B gồm có H2 và CO, tỉ khối của hỗn hợp khí B đốí với hiđro là 3,6.
a) Tính thành phần phần trăm theo thể tích các khí trong hỗn hợp A và hỗn hợp B.
b) Tính số mol hỗn hợp khí A cần dùng để đốt cháy hoàn toàn 1 mol hỗn hợp khí B. Các thể tích khí được đo trong cùng điều kiện nhiệt độ, áp suất.
Lời giải:
a) Gọi số mol O2 và O3 lần lượt là a moi và b mol.
Xét 1 mol hỗn hợp => a + b = 1 (*)
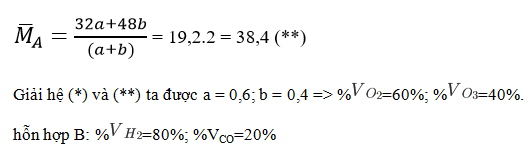
b) 2H2 + O2 → 2H2O (1)
2CO +O2 → 2CO2 (2)
3H2 + O3 → 3H2O (3)
3CO + O3 → 3CO2 (4)
Đặt số mol của A cần dùng để đốt cháy 1 mol B là x mol
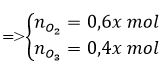
Trong 1 mol hỗn hợp B ta có:
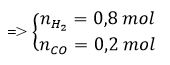
Từ (1), (2), (3) và (4):
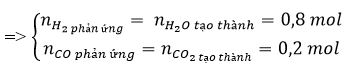
Áp dụng định luật bảo toàn khối lượng ta có:
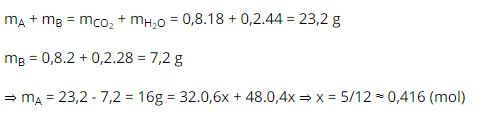
Tham khảo toàn bộ: Giải Hóa 10 nâng cao