Đề kiểm tra 45 phút Hóa 12 Chương 8 (đề 1)
Đề kiểm tra 45 phút Hóa 12 - Chương 8
Đề Số 1
Câu 1: Phản ứng nào sau đây đã được viết không đúng?
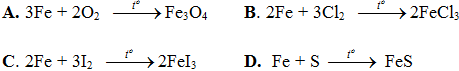
Câu 2: Kim loại có các tính chất vật lý chung là
A. Tính dẻo, tính dẫn điện, tính khó nóng chảy, ánh kim
B. Tính dẫn điện, tính dẫn nhiệt, ánh kim, tính đàn hồi
C. Tính dẻo, tính dẫn điện, tính dẫn nhiệt, ánh kim
D. Tính dẻo, tính dẫn điện, tính dẫn nhiệt, tính cứng
Câu 3: Kim loại nào sau đây có độ cứng lớn nhất trong số tất cả các kim loại?
A. W (vonfam) B. Fe (sắt) C. Cr (crom) D. Cu (đồng).
Câu 4: Ứng dụng của crom là?
A. Crom là kim loại rất cứng có thể dùng làm mũi khoan đá.
B. Crom làm hợp kim cứng và chịu nhiệt hơn,nên dùng để tạo thép cứng,không gỉ, chịu nhiệt.
C. Crom là kim loại nhẹ, nên được sử dụng tạocác hợp kim dùng trong ngành hàng không.
D. Điều kiện thường, crom tạo được dùng làm tế bào quang điện.
Câu 5: Hòa tan hết 18,8 g hh gồm Cr và Fe trong dd HCl loãng sau phản ứng thu được 7,84 lít khí (đktc). Khối lượng Cr trong hỗn hợp là
A. 8,4 g. B . 10,4 g. C. 7,8g. D. 5,2g.
Câu 6:Dãy gồm các kim loại đều tác dụng với H2SO4 loãng là:
A. Na, Al, Cu, Mg B. Na, Fe, Cu, Ba, Mg
C. Al, Mg, Fe, Na, Ba D. Ba, Na, Al, Ag
Câu 7: Số electron lớp ngoài cùng của các nguyên tử kim loại thuộc nhóm IA là
A.1 B. 2. C. 3. D. 4.
Câu 8:Cho các ion: Fe2+ (1); Ag+ (2); Cu2+ (3). Thứ tự tăng dần tính oxi hoá của các ion đó là:
A. (2) < (3) < (1). B. (1) < (2) < (3).
C. (1) < (3) < (2). D. (2) < (1) < (3).
Câu 9: Khi nối dây điện bằng nhôm với dây điện bằng đồng để ngoài trời trong môi trường không khí ẩm thì ở mối nối, kim loại nào sẽ bị ăn mòn nhanh do hiện tượng ăn mòn điện hóa?
A. Cu bị ăn mòn điện hóa. B. Al bị ăn mòn điện hóa.
C. Cả 2 kim loại đều cùng lúc bị ăn mòn. D. Không có kim loại nào bị ăn mòn điện hóa.
Câu 10: Cấu hình electron của Fe2+ là
A. 1s22s22p63s23p63d5. B. 1s22s22p63p6.
C. 1s22s22p63s2. D. 1s22s22p63s23p63d6.
Câu 11: Cho m gam bột Fe vào 200ml dung dịch HCl 0,4M và Cu(NO3)2 0,2M. Lắc đều cho các phản ứng xảy ra hoàn toàn, sau phản ứng thu được hỗn hợp chất rắn có khối lượng bằng 0,75m gam và V lít (ở đktc) khí NO (sản phẩm khử duy nhất của N+5). Giá trị của m là
A. 9,31 và 2,24. B. 5,44 và 0,448. C. 5,44 và 0,896. D. 3,84 và 0,448.
Câu 12: Chất dùng để làm mềm nước cứng tạm thời là
A. CaCl2. B. Ca(OH)2. C. HCl. D. Ca(HCO3)2.
Câu 13: Thạch cao nung có thành phần hoá học là:
A. CaSO4.H2O. B. Ca(OH)2. C. CaSO4.2H2O. D. CaSO4.
Câu 14: Nhận xét về tính chất hóa học của các hợp chất Fe (III) nào dưới đây là đúng?
|
|
Hợp chất |
Tính oxi hóa - khử |
|
A. |
Fe2O3 |
Chỉ có tính axit |
|
B. |
Fe(OH)3 |
Chỉ có tính khử |
|
C. |
FeCl3 |
Vừa oxi hóa vừa khử |
|
D. |
Fe2(SO4)3 |
Chỉ có tính oxi hóa |
Câu 15: Nước cứng là nước có chứa nhiều cation
A. Ca2+, Mg2+. B. Na+, K+. C. Cu2+, Fe3+. D. Al3+, Fe3+.
Câu 16: Nhôm bền trong môi trường không khí và nước là do
A. Có màng hidroxit Al(OH)3 bền vững bảo vệ B. Nhôm là kim loại kém hoạt động
C. Nhôm có tính thụ động với không khí và nước D.Có màng oxit Al2O3 bền vững bảo vệ
Câu 17: Hoà tan hoàn toàn 2,6 gam hai kim loại kiềm ở hai chu kì kế tiếp nhau vào nước thu được 1,12 lít H2 (đktc) bay ra. Hai kim loại đó là:
A. Li và Na. B. Na và K. C. K và Rb. D. Rb và Cs
Câu 18: Nhúng thanh Fe vào dung dịch CuSO4 quan sát thấy hiện tượng gì?
A. Thanh Fe có màu trắng và dung dịch nhạt màu xanh.
B. Thanh Fe có màu đỏ và dung dịch nhạt màu xanh.
C. Thanh Fe có màu trắng xám và dung dịch có màu xanh.
D. Thanh Fe có màu đỏ và dung dịch có màu xanh.
Câu 19: Để thu được m gam Cr từ Cr2O3 bằng phản ứng nhiệt nhôm (H = 70%) cần dùng 8,1 g nhôm. Khối lượng Crom thu được là:
A. 15,6 gam. B. 10,4 gam. C. 10,92 gam. D. 22,23 gam.
Câu 20: Cho 0,04 mol bột sắt vào dung dịch chứa 0,07 mol AgNO3. Khi phản ứng hoàn toàn thì khối lượng chất rắn thu được bằng:
A. 1,12 gam B. 4,32 gam C. 6,48 gam D. 7,56 gam
Câu 21: Hai oxit nào sau đây đều bị khử bởi CO ở nhiệt độ cao?
A. Al2O3 và ZnO. B. ZnO và K2O. C. Fe2O3 và MgO. D. FeO và CuO.
Câu 22: Cho sơ đồ chuyển hoá sau:![]() . Công thức của X, Y, Z lần lượt là
. Công thức của X, Y, Z lần lượt là
A. HCl, HNO3, Na2CO3. B.Cl2, HNO3, CO2.
C. HCl, AgNO3, (NH4)2CO3. D. Cl2, AgNO3, Mg(NO3)2.
Câu 23: Cho 46,8 g hỗn hợp bột Al và Al2O3 tác dụng với dung dịch NaOH dư thoát ra 20,16 lit H2 (đktc). Tính % khối lượng mỗi chất trong hỗn hợp ban đầu ?
A. 36% Al; 64% Al2O3 B. 34,6% Al; 65,4% Al2O3
C. 17,3% Al; 82,7% Al2O3 D. 32,4% Al; 67,6% Al2O3
Câu 24: Nhỏ 170 ml dung dịch NaOH 2M vào 100 ml dung dịch AlCl3 1M. Phản ứng hoàn toàn, lượng kết tủa thu được là:
A. 8,84g B. 7,8g C. 3,12g D. 4,68g
Câu 25: Nhúng thanh Fe nặng m gam vào 300 ml dung dịch CuSO4 1M, sau một thời gian thu được dung dịch X có chứa CuSO4 0,5M, đồng thời khối lượng thanh Fe tăng 4% so với khối lượng ban đầu. Giả sử thể tích dung dịch không thay đổi và lượng Cu sinh ra bám hoàn toàn vào thanh sắt. Giá trị m là
A. 24. B. 30. C. 32. D. 48.
Câu 26: Nhỏ từ từ cho đến dư dung dịch NaOH vào dung dịch AlCl3. Hiện tượng xảy ra là :
A. có kết tủa keo trắng và có khí bay lên. B. có kết tủa keo trắng, sau đó kết tủa tan.
C. không có kết tủa, có khí bay lên. D. chỉ có kết tủa keo trắng
Câu 27: Sục 4,48 lít CO2 (đkc) vào dung dịch Ca(OH)2 dư thì thu được khối lượng kết tủa là:
A. 19,7 gam. B. 40 gam. C. 20 gam. D. 39,4 gam.
Câu 28: Kim loại tác dụng với dung dịch NaOH ở điều kiện thường là kim loại nào trong các kim loại dưới đây:
A. Au. B. Cu. C. Al. D. Fe.
Câu 29: Tiến hành thí nghiệm: Cho 5,4 gam Al tác dụng hoàn toàn với dung dịch HNO3 dư tạo ra V lít khí NO (ở điều kiện tiêu chuẩn, giả sử NO là sản phẩm khử duy nhất ở thí nghiệm trên). V có giá trị là:
A. 2,24 lít. B. 4,48 lít. C. 5,6 lít. D. 6,72 lít.
Câu 30: Chất khử dạng khí để dùng sản xuất gang trong lò cao luyện gang chủ yếu là :
A. C. B. CaCO3. C. CO. D. CO2.
Câu 31: Cho 11,2 gam sắt vào dung dịch H2SO4 loãng dư, sau khi phản ứng xảy ra hoàn toàn với hiệu suất 100% thì số mol khí H2 thoát ra là:
A. 0,1 mol. B. 0,2 mol. C. 0,3 mol. D. 0,4 mol.
Câu 32: Tiến hành các thí nghiệm sau:
(a) Điện phân MgCl2 nóng chảy.
(b) Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3 dư.
(c) Nhiệt phân hoàn toàn CaCO3.
(d) Cho kim loại Na vào dung dịch CuSO4 dư.
(e) Dẫn khí H2 dư đi qua bột CuO nung nóng.
Sau khi các phản ứng kết thúc, số thí nghiệm thu được kim loại là
A. 3. B. 4. C. 1. D. 2.
Câu 33: Thổi khí CO dư qua 1,6 gam Fe2O3 nung nóng đến phản ứng hoàn toàn. Tính khối lượng Fe thu được.
A. 0,56 gam B. 1,12 gam C. 4,80 gam 11,2 gam
Câu 34: Cho sơ đồ chuyển hoá (mỗi mũi tên là một phương trình hóa học) ![]()
X, Y, Z lần lượt là
A. FeCl3, CuSO4, Ba(NO3)2. B.FeCl3, H2SO4(loãng), BaCl2.
C. FeCl2, H2SO4 (đặc, nóng), BaCl2. D. FeCl2, H2SO4 (loãng), Ba(NO3)2.
Câu 35: Cho dãy các chất : Cr(OH)3, Fe(NO3)3, (NH4)2CO3, NaHS, Cr2O3, Al, Al2O3. Số chất trong dãy có tính chất lưỡng tính là
A. 5 B. 2 C. 3 D. 4
Câu 36: Cho 33,1 gam hỗn hợp các kim loại Al, Cr, Fe tác dụng với lượng dư dung dịch HCl loãng nóng (trong điều kiện không có không khí), thu được dung dịch X và 6,72 lít khí H2 (ở đktc). Cô cạn dung dịch X được m gam muối khan. Giá trị của m là
A. 43,75. B. 55,5. C. 48,8. D. 54,4
Câu 37: H2O có thể tác dụng với tất cả các kim loại nào sau đây ở nhiệt độ thường?
A. Li, Na, K, Cu, Ba. B. Li, K, Ag, Ba.
C. Li, K, Na , Ba, Ca. D. Li, Na, Mg, Cu.
Câu 38: Hiện tượng xảy ra khi cho Ba vào dung dịch (NH4)2SO4 là
A. Có kết tủa trắng và có khí mùi khai bay lên. B. Chỉ có khí mùi khai thoát ra.
C. Chỉ có kết tủa trắng. D. Không có hiên tượng gì.
Câu 39: Hoà tan mẫu hợp kim Ba – K vào nước được dd A và có 6,72 lít H2 bay ra (đktc). Cần dùng bao nhiêu ml dung dịch HCl 1M để trung hoà hoàn toàn 1/10 dung dịch A (ml)
A. 60 B. 600 C. 40 D. 750
Câu 40: Chọn phát biểu đúng trong các phát biểu sau:
A. Nhôm là kim loại lưỡng tính. B. Al(OH)3 là bazơ lưỡng tính.
C. Al2O3 là oxit trung tính. D. Al(OH)3 là một hiđroxit lưỡng tính.
Đáp án và thang điểm
Mỗi câu trả lời đúng được 0,25 điểm, 0,25 x 40 = 10 điểm
|
Câu |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
Đáp án |
C |
B |
C |
B |
B |
C |
A |
C |
B |
D |
B |
B |
A |
D |
A |
D |
B |
B |
C |
D |
|
Câu |
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
29 |
30 |
31 |
32 |
33 |
34 |
35 |
36 |
37 |
38 |
39 |
40 |
|
Đáp án |
C |
C |
B |
D |
B |
B |
C |
C |
B |
C |
B |
A |
B |
B |
A |
D |
C |
A |
A |
D |
Tham khảo toàn bộ: Đề kiểm tra, đề thi Hóa 12 học kì 2
