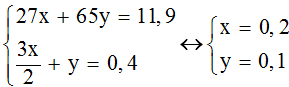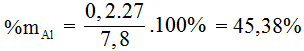Đề kiểm tra 1 tiết Hóa 10 Chương 5 - Đề 2
Đề kiểm tra 1 tiết Hóa 10 Chương 5 - Đề 2
Đề bài
Câu 1: Chất nào sau đây không thể dùng để làm khô khí hiđro clorua?
A. P2O5. C. Axit sunfuric đậm đặc.
C. NaOH rắn. D. CaCl2 khan.
Câu 2: Không đựng dung dịch axit nào sau đây trong bình thủy tinh:
A. Axit HCl B. Axit HNO3
C. Axit HF D. Axit H2SO4
Câu 3: Thứ tự giảm dần tính oxi hóa của halogen là
A. F2 > Cl2 > Br2 >I2. B. I2 >Br2 > Cl2 >F2.
C. Cl2> Br2 > I2 > F2. D. Br2 >I2 >Cl2 > F2.
Câu 4: Ở điều kiện thường, khí hiđro clorua là chất khí, không màu và nặng hơn không khí
A. 1,2586 lần. B. 2,45 lần. C. 1,2658 lần. D. 2,25 lần.
Câu 5: Trong công nghiệp người ta thường điều chế clo bằng cách
A. điện phân nóng chảy NaCl.
B. điện phân dung dịch NaCl có màng ngăn.
C. phân huỷ khí HCl.
D. cho HCl đặc tác dụng với MnO2; KMnO4
Câu 6: Brom có lẫn một ít tạp chất là Một trong các hoá chất có thể loại bỏ clo ra khỏi hỗn hợp là
A. KBr. B. KCl. C. H2O. D. NaOH.
II, Phần tự luận:
Bài 1:
a, Trình bày tính chất hóa học của Br2 ? Lấy ví dụ.
b, Viết các phương trình phản ứng xảy ra cho các sơ đồ sau (ghi rõ điều kiện phản ứng nếu có ):
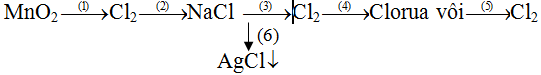
Bài 2: Hòa tan 11,9 gam hỗn hợp bột 2 kim loại Al, Zn bởi m g dung dịch HCl 20% vừa đủ thu được 8,96 lít H2 (đktc).
a, Tính % khối lượng mỗi kim loại trong hỗn hợp ban đầu.
b, Tính m ?
(Cho Al = 27, Zn = 65, Cl = 35,5 )
Đáp án và thang điểm
I, Phần trắc nghiệm:
|
Câu |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
Đáp án |
B |
D |
C |
C |
D |
B |
A |
B |
II, Phần tự luận:
Bài 1:
Chú ý:
- Học sinh làm bài theo cách khác kết quả đúng vẫn cho đủ điểm .
- Nếu cân bằng phương trình hoá học sai thì trừ 1/2 số điểm của ptrình hoá học đó.
- Nếu viết sai công thức hoá học thì không cho điểm phương trình hoá học đó.
a, Trình bày tính chất hóa học của Br2 (0,5 điểm)
Lấy ví dụ (0,5 điểm)
b, Viết các phương trình phản ứng xảy ra cho các sơ đồ sau (ghi rõ điều kiện phản ứng nếu có ): Mỗi phương trình hoá học đúng được 0,25 điểm
Bài 2:
|
Đáp án |
Điểm |
|
nH2= 0,4 mol 2Al + 6HCl → 2AlCl3 + 3H2 x mol Zn + 2HCl → ZnCl2 + H2 ymol ymol
→%mMg = 100% - 45,38%= 54,62% m= 0,8.36,5.100%/20%= 146 g |
0,5 đ’
0,5 đ’
0,5 đ’
0,5 đ’
0,5 đ’
0,5 đ’ 1 đ’ |
Tham khảo toàn bộ: Đề kiểm tra, đề thi Hóa 10 học kì 2