Ăn mòn hóa học là gì và ăn mòn điện hóa là gì? Bản chất và ví dụ
Ăn mòn là kẻ thù lớn nhất mà kim loại phải đối mặt, đó là sự xuất hiện gây ra bởi phản ứng của kim loại và các yếu tố môi trường khác nhau. Trong hóa học, ăn mòn được chia thành 2 kiểu là ăn mòn hóa học và ăn mòn điện hóa học. Rất nhiều bạn học sinh bị nhầm lãn giữa 2 khái niệm này, vậy hãy cùng Toploigiai tìm hiểu về Ăn mòn hóa học và ăn mòn điện hóa qua bài viết sau đây nhé!
Thế nào hiện tượng ăn mòn
Hiện tượng ăn mòn là sự phá hủy dần ần các vật liệu dựa trên các phản ứng hóa học giữa các chất hoặc phản ứng điện hóa học với môi trường chứa vật thể đó.
Trong các nhà máy lớn, các thiết bị, máy móc, các kết cấu công trình, các vật liệu kim loại.... Sau một thời gian dài làm việc, hay bảo quản bị hư hỏng hoặc hoen gỉ.
Quá trình ăn mòn diễn ra nhanh chóng tùy thuộc vào từng loại vật liệu hay do tăng tiếp xúc với không khí, nước hoặc các chất khác. Theo thời gian, sự ăn mòn làm giảm độ bền, tăng tính thấm đối với chất lỏng và khí, làm suy giảm các đặc tính hữu ích khác của vật liệu.
Thiệt hại do ăn mòn có thể gây ra như nứt, rò rỉ, rỗ và cuối cùng là hỏng hóc tài sản nếu vẫn không có biện pháp xử lý phù hợp, kịp thời.
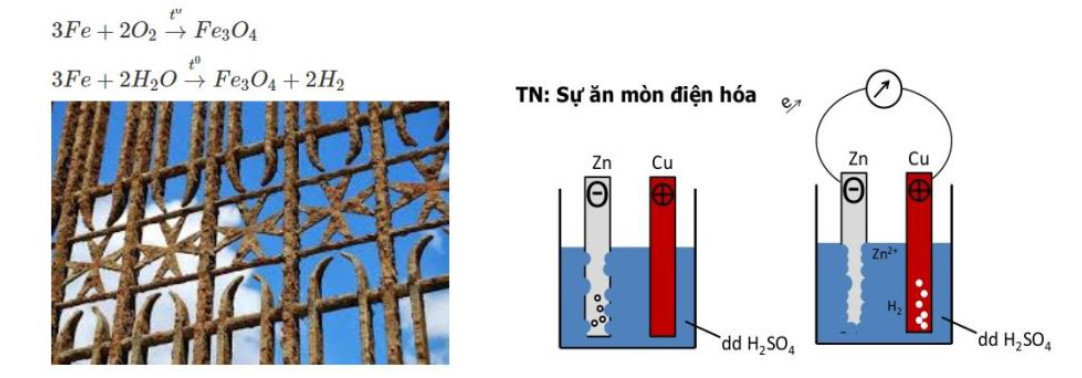
* Một số ví dụ đặc trưng cho quá trình ăn mòn ngoài tự nhiên:
- Thanh sắt để ngoài trời dần dần bị mòn.
- Chậu nhôm để ngoài trời lâu sẽ bị mòn, thủng . . .
- Đồ đồng để lâu trong nước bị mòn dần.
Ăn mòn hóa học là gì?
Ăn mòn hóa học là sự phá hủy dần dần bề mặt kim loại do phản ứng của bề mặt với các chất ở môi trường bên ngoài.
Bản chất ăn mòn hóa học
Bản chất của ăn mòn hóa học chính là một dang ăn mòn kim loại do tác động của môi trường xung quanh.
Ăn mòn hóa học xảy ra khi kim loại phản ứng với hơi nước hoặc chất khí ở nền nhiệt độ cao. Bản chất đây chính là quá trình oxy hóa khử. Quá trình oxy hóa khử diễn ra khi các electron của kim loại sẽ được chuyển đến các chất một cách trực tiếp trong môi trường.
Hiện tượng này thường xảy ra ở các kim loại ở máy móc hay các thiết bị phải tiếp xúc với hóa chất, hơi nước thường xuyên ở nhiệt độ cao hay khí oxy.
Ví dụ về sự ăn mòn hóa học
3Fe + 4H2O → Fe3O4 + 4H2
2Fe + 3Cl2 → 2FeCl3
3Fe + 2O2 → Fe3O4
Thực tế, ăn mòn hóa học thường xảy ra ở những bộ phận của thiết bị lò đốt và các thiết bị thường xuyên tiếp xúc với hơi nước và khí oxi...
Ngâm thanh trong chậu nước lâu ngày, dần thanh sắt sẽ bị rỉ sét. Bởi trong một khoảng thời gian dài thanh sắt sau khi tiếp xúc với oxi và độ ẩm sẽ tạo thành một hợp chất mới đó là rỉ sắt, trong đó nước là chất xúc tác tạo nên sự ăn mòn.
Ăn mòn điện hóa là gì?
Ăn mòn điện hóa là hiện tượng hai kim loại khác nhau tiếp xúc trực tiếp trong chất lỏng dẫn điện, một trong hai kim loại có thể bị ăn mòn.
Bản chất ăn mòn điện hóa
Sự ăn mòn điện hóa là sự phá hủy các kim loại khi hợp kim tiếp xúc với dung dịch chất điện ly và sản xuất ra dòng điện. Bản chất chính là quá trình oxy hóa khử, khi kim loại bị ăn mòn do tác dụng của dung dịch có chất điện ly và tạo là dòng electron chuyển dời từ âm sang dương.
Sự ăn mòn điện hóa xảy ra khi một cặp kim loại hay hợp kim nhúng vào dung dịch axit, nước muối hoặc ở ngoài không khí ẩm.
Cơ chế ăn mòn điện hóa
Gang hoặc thép là những hợp kim Fe-C, trong đó cực âm là những tinh thể Fe, cực dương là những tinh thể C. Các điện cực này tiếp xúc trực tiếp với nhau và với một dung dịch điện li phủ ngoài. Như vậy, vật bị ăn mòn theo kiểu điện hóa:
- Ở cực âm: Các nguyên tử Fe bị oxi hóa thành. Các ion này tan vào dung dịch điện li trong đó đã có một lượng không khí oxi, tại đây chúng bị oxi hóa tiếp thành.
- Ở cực dương: Các ion hiđro của dung dịch điện li di chuyển đến cực dương, tại đây chúng bị khử thành hiđro tự do, sau đó thoát ra khỏi dung dịch điện li
- Các tinh thể Fe lần lượt bị oxi hóa từ ngoài vào trong. Sau một thời gian, vật bằng gang (thép) sẽ bị ăn mòn hết.
Ví dụ ăn mòn điện hóa học
- Ăn mòn điện hóa là loại ăn mòn kim loại phổ biến và nghiêm trọng nhất, ví dụ:
- Cửa sắt tiếp xúc với không khí ẩm.
- Ống dẫn chôn dưới lòng đất.
- Phần vỏ tàu thủy ngập trong nước…

So sánh giữa ăn mòn điện hóa và ăn mòn hóa học
Phân loại |
Ăn mòn hóa học |
Ăn mòn điện hóa học |
Điều kiện xảy ra ăn mòn |
Thường xảy ra ở những thiết bị lò đốt hoặc những thiết bị thường xuyên phải tiếp xúc với hơi nước và khí oxi |
– Các điện cực phải khác nhau, có thể là cặp hai kim loại khác nhau hoặc cặp kim loại – phi kim hoặc cặp kim loại – hợp chất hóa học (như Fe3C). Trong đó kim loại có thế điện cực chuẩn nhỏ hơn sẽ là cực âm. – Các điện cực phải tiếp xúc trực tiếp hoặc gián tiếp với nhau qua dây dẫn, các điện cực phải tiếp xúc với dung dịch chất điện li. |
Cơ chế của sự ăn mòn |
Thiết bị bằng Fe tiếp xúc với hơi nước, khí oxi thường xảy ra phản ứng: 3Fe + 4H2O Fe3O4 + 4H2↑ 3Fe + 2O2 Fe3O4 |
– Sự ăn mòn điện hóa một vật bằng gang (hợp kim Fe – C)(hoặc thép) trong môi trường không khí ẩm có hòa tan khí CO2, SO2, O2… sẽ tạo ra một lớp dung dịch điện li phủ bên ngoài kim loại. – Tinh thế Fe (cực âm), tinh thể C là cực dương. Ở cực dương: xảy ra phản ứng khử: 2H+ + 2e → H2 ; O2 + 2H2O + 4e → 4OH- Ở cực âm: xảy ra phản ứng oxi hóa: Fe → Fe2+ + 2e Những Fe2+ tan vào dung dịch chứa oxi → Fe3+ và cuối cùng tạo gỉ sắt có thành phần Fe2O3.nH2O |
Bản chất của sự ăn mòn |
Là quá trình oxi hóa – khử, trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong môi trường, ăn mòn xảy ra chậm |
Là sự ăn mòn kim loại do tác dụng của dung dịch chất điện li và tạo nên dòng điện. Mòn điện hóa xảy ra nhanh hơn ăn mòn hóa học. |
Một số biện pháp chống ăn mòn
Ăn mòn là kẻ thù lớn nhất mà kim loại phải đối mặt. Bởi đó là sự xuất hiện gây ra bởi phản ứng của kim loại và các yếu tố môi trường khác nhau.
Ăn mòn làm ảnh hưởng đến vẻ ngoài của kim loại gây mất thẩm mỹ với các vật dụng dùng để trang trí. Hơn thế, ăn mòn ảnh hưởng đến hiệu suất về độ bền và khả năng chịu tải với các ứng dụng trong công nghiệp, xây dựng…
Hiện nay, có những phương pháp ngăn ngừa ăn mòn hiệu quả có thể kéo dài tuổi thọ của các thiết bị, công trình. Nhưng không phải tất cả các phương pháp chống ăn mòn đều như nhau. Chúng ta cần chọn đúng phương pháp dựa trên tính chất của từng kim loại và các yếu tố về môi trường.
Các biện pháp được sử dụng để chống ăn mòn:
- Sử dụng các kim loại không dễ bị ăn mòn: Nhôm và thép không gỉ, Titan,..
- Lớp phủ bảo vệ: Phủ một lớp sơn bảo vệ (sơn tĩnh điện) sẽ làm tăng tính thẩm mỹ cho kim loại và ngăn ngừa sự ăn mòn.
- Mạ kim loại: Phủ một lớp kim loại mỏng lên kim loại mà muốn bảo vệ. Lớp kim loại ngăn chặn sự ăn mòn và tăng thêm tính thẩm mỹ.
+ Mạ cơ học
+ Electroless – Phương pháp này sử dụng phản ứng hóa học để tạo lớp phủ kim loại như niken hoặc coban cho kim loại chính.
+ Nhúng nóng – Đây là một kỹ thuật phủ đơn giản đòi hỏi chất nền phải được ngâm trong bể kim loại bảo vệ nóng chảy. Tạo thành một lớp bảo vệ mỏng xung quanh kim loại nền.
- Sử dụng chất ức chế ăn mòn
+ Chất ức chế ăn mòn là hóa chất được áp dụng cho bề mặt kim loại. Phản ứng với kim loại hoặc khí xung quanh để ức chế hoặc triệt tiêu các quá trình điện hóa dẫn đến sự ăn mòn.
- Kiểm soát môi trường
+ Môi trường đóng một vai trò quan trọng trong quá trình ăn mòn. Bằng cách kiểm soát môi trường có thể ngăn ngừa hoặc giảm tốc độ ăn mòn.
Những giải pháp đơn giản bao gồm giảm tiếp xúc với độ ẩm, kiểm soát nồng độ oxy, lưu huỳnh hoặc clo.
